网址:http://m.1010jiajiao.com/timu3_id_192400[举报]
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。
(1)在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。
①
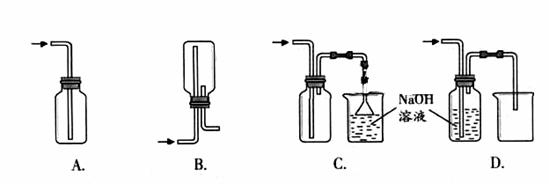 |
下列收集Cl2的正确装置是 。
②将Cl2通入水中,所得溶液中具有氧化性的含氯粒子是 。ks5u
③设计实验比较Cl2和Br2的氧化性,操作与现象是:取少量新制氯水和CCl4于试管中,
(2)能量之间可以相互转化:电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。设计两种类型的原电池,探究其能量转化效率。
 限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
限选材料:ZnSO4(aq),FeSO4(aq),CuSO4(aq);铜片,铁片,锌片和导线。
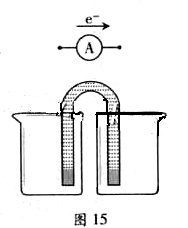
① 完成原电池的甲装置示意图(见图15),并作相应标注。
要求:在同一烧杯中,电极与溶液含相同的金属元素。
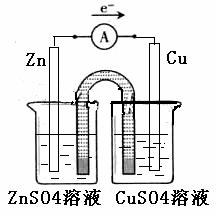
② 以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极 。
③ 甲乙两种原电池中可更有效地将化学能转化为电能的是 ,其原因是 。
(3)根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在(2)的材料中应选 作阳极。
查看习题详情和答案>>化学小组采用类似制乙酸乙酯的装置(如下图),用环己醇制备环己烯。
已知: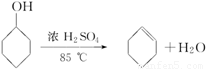
|
|
密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
|
环己醇 |
0.96 |
25 |
161 |
能溶于水 |
|
环己烯 |
0.81 |
-103 |
83 |
难溶于水 |
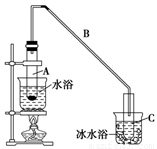
(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片(防止爆沸),缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用________(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液
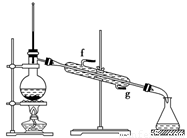
②再将环己烯按上图装置蒸馏,冷却水从________口进入(填“g”或“f”)。蒸馏时要加入生石灰,其目的是_____________________________________。
③收集产品时,控制的温度应在________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是________。
A.蒸馏时从70 ℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________。
A.分别加入酸性高锰酸钾溶液
B.分别加入用金属钠
C.分别测定沸点
查看习题详情和答案>>
化学小组采用类似制乙酸乙酯的装置(如下图),用环己醇制备环己烯。
已知:
| | 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |

(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片(防止爆沸),缓慢加热至反应完全,在试管C内得到环己烯粗品。
①导管B除了导气外还具有的作用是________。
②试管C置于冰水浴中的目的是______________________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在________层(填“上”或“下”),分液后用________(填入编号)洗涤。
A.KMnO4溶液 B.稀H2SO4 C.Na2CO3溶液

②再将环己烯按上图装置蒸馏,冷却水从________口进入(填“g”或“f”)。蒸馏时要加入生石灰,其目的是_____________________________________。
③收集产品时,控制的温度应在________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是________。
A.蒸馏时从70 ℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是________。
A.分别加入酸性高锰酸钾溶液
B.分别加入用金属钠
C.分别测定沸点 查看习题详情和答案>>
(1)P、S、Cl三种元素中,第一电离能最小的是______.
(2)PCl3和CH4中心原子的杂化类型相同,PCl3分子的空间构型是______.
(3)钛原子的电子排布式为______.在浓的TiCl3溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3?6H2O的绿色晶体,将1mol该物质溶于水,加入足量硝酸银溶液,立即产生1mol氯化银沉淀,则该配合物阳离子的化学式为______,形成该离子时提供孤电子对的分子或离子是______(填化学式).
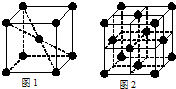
(4)铁元素在1183K以下形成的晶体的基本结构单元如图1所示,1183K以上转变为图2所示结构的基本结构单元.两种晶体的基本结构单元中的原子个数之比为______.
(1)下列关于实验的叙述正确的有 .
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.滴定实验中用的移液管、锥形瓶和滴定管都要用所盛溶液润洗
C.做完酚醛树脂实验的试管可用乙醇浸泡后清洗.
D.酸性高锰酸钾溶液一般用盐酸酸化,可除去乙烯中混有的二氧化硫气体
E.除去氯化镁溶液中含有的FeCl3 杂质,可采用加入MgO调节pH除去.
F.蒸发操作时,用玻璃棒不断搅拌,防止液体飞溅出来,等水分完全蒸干后,停止加热
G.可用移液管量取0.10mol/L 的KMnO4溶液25.10mL
H.用pH试纸测得某新制氯水的pH值为3
(2 ) 下列实验没有错误的是

(3)如图1为常见仪器的部分结构(有的仪器被放大)
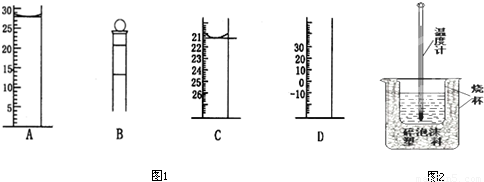
A图中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为NmL,仰视时读数为M mL,若M>N,则所使用的仪器是 (填字母标号).
(4)中和热的测定如图2所示,该装置图中有两处实验用品没有画出,它们是烧杯上方的泡沫塑料盖和 .完成一次中和热测定实验,温度计至少要使用 次. 查看习题详情和答案>>