摘要:A.B.C.D是上述列举的物质中的四种物质.它们有如下的转化关系: (1)写出A.B.C.D四种物质的化学式 A B C D (2)写出甲.乙.丙.丁所表示的反应物的化学式或反应条件 甲 乙 丙 丁
网址:http://m.1010jiajiao.com/timu3_id_190818[举报]
海水是人类宝贵的自然资源,从海水中可以提取多种化工原料,下图是某工厂对海水资源综合利用的示意图:
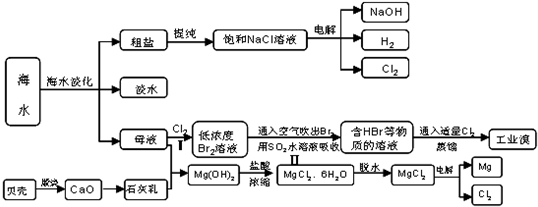
(1)请列举海水淡化的两种方法______、______.
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:______.步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式______
(3)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2?6H2O的原因______
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是______
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(5)从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目的______.
(6)上述工艺中可以得到金属Mg,请写出工业上制备金属铝的化学方程式______.
查看习题详情和答案>>

(1)请列举海水淡化的两种方法______、______.
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是:______.步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式______
(3)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2?6H2O的原因______
(4)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用做镁蒸气的冷却剂的是______
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
(5)从各种经营综合开发,打造大而强的现代企业以及本厂生产所需要的原料等方面来看,你认为该化工厂还可以再增加的生产项目的______.
(6)上述工艺中可以得到金属Mg,请写出工业上制备金属铝的化学方程式______.
化学变化中既有物质变化,也有能量变化,研究化学反应有利于指导工业生产.下列是常见的化学反应:①电解熔融氯化钠 ②氮气与氢气合成氨气 ③锌与稀硫酸反应 ④煅烧石灰石.
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是
a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率
查看习题详情和答案>>
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是
②③
②③
(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是④
④
;从反应前后物质种类的变化角度看,①和④均属于分解
分解
反应;①和②在变化过程中断裂的化学键类型分别为离子键
离子键
、共价键
共价键
.(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是
c
c
.a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是
锌
锌
,电子流向正
正
极.(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率
增大
增大
(填“增大”、“减小”或“不变”,下同),逆反应速率增大
增大
;请列举一项该反应达到平衡的标志正反应速率等于逆反应速率
正反应速率等于逆反应速率
.
化学变化中既有物质变化,也有能量变化,研究化学反应有利于指导工业生产.下列是常见的化学反应:①电解熔融氯化钠 ②氮气与氢气合成氨气 ③锌与稀硫酸反应 ④煅烧石灰石.
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是______(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是______;从反应前后物质种类的变化角度看,①和④均属于______反应;①和②在变化过程中断裂的化学键类型分别为______、______.
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是______.
a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是______,电子流向______极.
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率______(填“增大”、“减小”或“不变”,下同),逆反应速率______;请列举一项该反应达到平衡的标志______.
查看习题详情和答案>>
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是______(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是______;从反应前后物质种类的变化角度看,①和④均属于______反应;①和②在变化过程中断裂的化学键类型分别为______、______.
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是______.
a.加入硝酸,增大氢离子的浓度 b.用浓硫酸代替稀硫酸
c.加入少量铜粉 d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是______,电子流向______极.
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率______(填“增大”、“减小”或“不变”,下同),逆反应速率______;请列举一项该反应达到平衡的标志______.
查看习题详情和答案>>
化学变化中既有物质变化,也有能量变化,研究化学反应有利于指导工业生产.下列是常见的化学反应:①电解熔融氯化钠②氮气与氢气合成氨气③锌与稀硫酸反应④煅烧石灰石.
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是______(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是______;从反应前后物质种类的变化角度看,①和④均属于______反应;①和②在变化过程中断裂的化学键类型分别为______、______.
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是______.
a.加入硝酸,增大氢离子的浓度b.用浓硫酸代替稀硫酸
c.加入少量铜粉d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是______,电子流向______极.
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率______(填“增大”、“减小”或“不变”,下同),逆反应速率______;请列举一项该反应达到平衡的标志______.
查看习题详情和答案>>
(1)从不同角度可以对上述反应进行分类:从反应前后能量变化角度看上述反应属于放热反应的是______(填序号,下同);从有无电子转移角度看上述反应属于非氧化还原反应的是______;从反应前后物质种类的变化角度看,①和④均属于______反应;①和②在变化过程中断裂的化学键类型分别为______、______.
(2)反应③在实验室中用于制备氢气,要提高生成氢气的速率下列措施合理的是______.
a.加入硝酸,增大氢离子的浓度b.用浓硫酸代替稀硫酸
c.加入少量铜粉d.将稀硫酸的体积加倍.
反应③可以设计成原电池反应,其中负极上反应的物质是______,电子流向______极.
(3)反应②是可逆反应,常应用于工业生产,升高温度正反应速率______(填“增大”、“减小”或“不变”,下同),逆反应速率______;请列举一项该反应达到平衡的标志______.
我们已经学过了很多物质,如氧气、钠、硫酸、铁、碳酸钙、氢氧化钠、氢氧化铁、氯化铝、过氧化钠、氯化钠、氢氧化铝、碳酸钠、盐酸、碳酸氢钠、氧化铁、氧化钠、氧化铝、氯化铁、铝、二氧化碳、偏铝酸钠、二氧化硫等
(1)以上列举的物质中,属于两性氧化物的是
(2)A、B、C、D是上述列举的物质中的四种物质,它们有如下的转化关系:
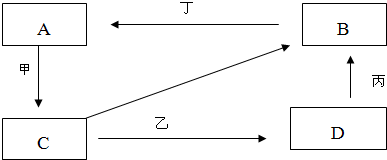
①写出A、B、C、D四种物质的化学式:A
②写出甲、乙、丙、丁所表示的反应物的化学式或反应条件
甲
(3)从以上列举的物质中选择合适的物质,在溶液中分别发生如下的离子反应.写出其离子方程式.
①有一种难溶物质生成
②有一种气体物质生成
③有一种弱电解质生成
查看习题详情和答案>>
(1)以上列举的物质中,属于两性氧化物的是
氧化铝
氧化铝
(2)A、B、C、D是上述列举的物质中的四种物质,它们有如下的转化关系:

①写出A、B、C、D四种物质的化学式:A
Al2O3
Al2O3
BAlCl3
AlCl3
CNaAlO2
NaAlO2
DAl(OH)3
Al(OH)3
②写出甲、乙、丙、丁所表示的反应物的化学式或反应条件
甲
NaOH
NaOH
乙CO2
CO2
丙HCl
HCl
丁加热
加热
(3)从以上列举的物质中选择合适的物质,在溶液中分别发生如下的离子反应.写出其离子方程式.
①有一种难溶物质生成
Fe3++3OH-=Fe(OH)3↓
Fe3++3OH-=Fe(OH)3↓
②有一种气体物质生成
HCO3-+H+=CO2↑+H2O
HCO3-+H+=CO2↑+H2O
③有一种弱电解质生成
Al2O3+6H+=2Al3++3H2O
Al2O3+6H+=2Al3++3H2O
.