摘要:15.铝和氧化铁在高温下发生的反应中.铝是 A.氧化剂 B.还原剂 C.既不是氧化剂又不是还原剂 D.既是氧化剂又是还原剂
网址:http://m.1010jiajiao.com/timu3_id_190478[举报]
铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨.现取不同质量的该铝热剂分别和100mL同浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如下表(气体体积均在标准状况下测定).
(1)该铝热反应的化学方程式为
(2)该铝热剂中加入NaOH溶液时发生反应的化学方程式为
(3)求NaOH溶液的物质的量浓度:
(4)求该铝热剂中铝的质量分数.
查看习题详情和答案>>
| ① | ② | ③ | |
| 铝热剂质量/g | 7.5 | 18.0 | 20.0 |
| 气体体积/L | 3.36 | 6.72 | 6.72 |
2Al+Fe2O3
2Fe+Al2O3
| ||
2Al+Fe2O3
2Fe+Al2O3
| ||
(2)该铝热剂中加入NaOH溶液时发生反应的化学方程式为
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(3)求NaOH溶液的物质的量浓度:
(4)求该铝热剂中铝的质量分数.
钠、铝和铁是三种重要的金属.请回答:
(1)三种金属中,
(2)三种金属在一定条件下均能与水发生反应.其中,铁与水蒸气反应的化学方程式为
a.钠沉入水底 b.钠熔成小球 c.钠四处游动 d.溶液变为红色.
查看习题详情和答案>>
(1)三种金属中,
铝
铝
既能与盐酸又能与氢氧化钠溶液反应,且生成物均为盐和氢气.写出该物质与氢氧化钠溶液反应的化学方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)三种金属在一定条件下均能与水发生反应.其中,铁与水蒸气反应的化学方程式为
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
.钠与水反应时可观察到的实验现象有
| ||
bc
bc
(填序号).在实验室中,通常将金属钠保存在煤油
煤油
中;钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑
2Na+2H2O=2NaOH+H2↑
a.钠沉入水底 b.钠熔成小球 c.钠四处游动 d.溶液变为红色.
 (12分)某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金。
(12分)某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金。
(1)写出铝和氧化铁在高温下反应的化学方程式: ▲ 。
(2)设计一个最简单的实验方案,证明上述所得的块状熔融物中含有金属铝。写出表示该实验原理的离子方程式: ▲ 。
(3)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充 www..com
分反应,发现反应过程中无气体放出。在反应结束后的溶
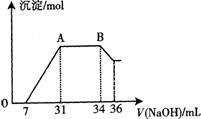
液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为 ▲ mol。
②熔融物中金属铝和金属铁的物质的量的之比为 ▲ 。
查看习题详情和答案>>某同学通过查阅资料得知:铝和氧化铁在高温下反应所得到的熔融物应该是铁铝合金.
(1)写出铝和氧化铁在高温下反应的化学方程式:______.
(2)设计一个最简单的实验方案,证明上述所得的熔融物中含有金属铝.写出表示该实验原理的离子方程式:______.
(3)某同学取一定量上述熔融物与过量的且很稀的硝酸充分反应,发现反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.在AB段,有刺激性气味的气体产生.试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为______mol.
②熔融物中金属铝和金属铁的物质的量之比为______.

查看习题详情和答案>>
(1)写出铝和氧化铁在高温下反应的化学方程式:______.
(2)设计一个最简单的实验方案,证明上述所得的熔融物中含有金属铝.写出表示该实验原理的离子方程式:______.
(3)某同学取一定量上述熔融物与过量的且很稀的硝酸充分反应,发现反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.在AB段,有刺激性气味的气体产生.试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为______mol.
②熔融物中金属铝和金属铁的物质的量之比为______.
