摘要:17.能证明浓硫酸具有强氧化性的事实是 A.常温下浓硫酸可用铝.铁制容器盛装 B.不能用浓硫酸干燥氨气 C.与NaCl反应制HCl D.与Na2SO3反应制SO2
网址:http://m.1010jiajiao.com/timu3_id_190114[举报]
实验室可以用乙醇和浓硫酸在170 ℃制乙烯,化学反应原理:CH3CH2OH CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):
CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个): 
(1)验证乙醇与浓硫酸混合反应副产物有二氧化硫和二氧化碳:
①选择必要装置连接顺序:a→ →f→g→e→d→b(填接口序号);
②确认混合气体中有二氧化碳存在的实验依据是
(2)若制备1,2-二溴乙烷的装置为A→E→C→D,
①D中的反应现象为
②分离1,2-二溴乙烷的操作中使用的玻璃仪器有_____________________________
③有同学建议在A、E之间增加G装置,其作用是
(3)阅读资料知,“酸性高锰酸钾溶液能氧化乙烯生成二氧化碳”。请你设计方案验证资料真实性:
①装置的连接顺序:A→____________________(填装置序号)。
②能证明上述资料符合事实的实验现象是_______________________。
(4)为了探究乙烯与溴水的反应是取代反应还是加成反应,该同学进行如下实验:①测定D瓶中溴水的pH; ②将纯净的乙烯通入D至溶液完全退色;③________。
实验室可以用乙醇和浓硫酸在170 ℃制乙烯,化学反应原理:CH3CH2OH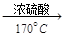 CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):
CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):

(1)验证乙醇与浓硫酸混合反应副产物有二氧化硫和二氧化碳:
①选择必要装置连接顺序:a→ →f→g→e→d→b(填接口序号);
②确认混合气体中有二氧化碳存在的实验依据是
(2)若制备1,2-二溴乙烷的装置为A→E→C→D,
①D中的反应现象为
②分离1,2-二溴乙烷的操作中使用的玻璃仪器有_____________________________
③有同学建议在A、E之间增加G装置,其作用是
(3)阅读资料知,“酸性高锰酸钾溶液能氧化乙烯生成二氧化碳”。请你设计方案验证资料真实性:
①装置的连接顺序:A→____________________(填装置序号)。
②能证明上述资料符合事实的实验现象是_______________________。
(4)为了探究乙烯与溴水的反应是取代反应还是加成反应,该同学进行如下实验:①测定D瓶中溴水的pH; ②将纯净的乙烯通入D至溶液完全退色;③________。
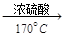 CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个):
CH2=CH2↑+H2O,由于浓硫酸具有强氧化性,其副产物有二氧化硫和二氧化碳等。某同学根据上述信息和实验目标选择下列实验装置设计实验探究(每种装置都有若干个): 
(1)验证乙醇与浓硫酸混合反应副产物有二氧化硫和二氧化碳:
①选择必要装置连接顺序:a→ →f→g→e→d→b(填接口序号);
②确认混合气体中有二氧化碳存在的实验依据是
(2)若制备1,2-二溴乙烷的装置为A→E→C→D,
①D中的反应现象为
②分离1,2-二溴乙烷的操作中使用的玻璃仪器有_____________________________
③有同学建议在A、E之间增加G装置,其作用是
(3)阅读资料知,“酸性高锰酸钾溶液能氧化乙烯生成二氧化碳”。请你设计方案验证资料真实性:
①装置的连接顺序:A→____________________(填装置序号)。
②能证明上述资料符合事实的实验现象是_______________________。
(4)为了探究乙烯与溴水的反应是取代反应还是加成反应,该同学进行如下实验:①测定D瓶中溴水的pH; ②将纯净的乙烯通入D至溶液完全退色;③________。
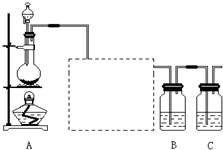 已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
已知非金属单质硫(S)是淡黄色固体粉末,难溶于水.为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:(1)装置A的分液漏斗中盛装的试剂是
浓盐酸
浓盐酸
,烧瓶中加入的试剂是MnO2
MnO2
.(2)画出虚线框内的实验装置图,并注明所加试剂,


除去Cl2中的HCl气体
除去Cl2中的HCl气体
.(3)装置B中盛放的试剂是
A
A
(选填下列所给试剂的代码),实验现象为有淡黄色沉淀生成
有淡黄色沉淀生成
,化学反应方程式是Na2S+Cl2=2NaCl+S↓
Na2S+Cl2=2NaCl+S↓
,该反应属于四种基本反应类型中的置换
置换
反应.A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因.
Cl原子、S原子的电子层数相同,但最外层电子数Cl原子是7,S原子是6,且原子半径Cl<S,因此,在反应中Cl原子比S原子更容易获得电子达稳定结构,故氯元素的非金属性比硫元素的非金属性强.
Cl原子、S原子的电子层数相同,但最外层电子数Cl原子是7,S原子是6,且原子半径Cl<S,因此,在反应中Cl原子比S原子更容易获得电子达稳定结构,故氯元素的非金属性比硫元素的非金属性强.
(5)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例).
HCl的稳定性比H2S的稳定性强或者HClO4的酸性比H2SO4的酸性强.(其他合理答案均可)
HCl的稳定性比H2S的稳定性强或者HClO4的酸性比H2SO4的酸性强.(其他合理答案均可)
(6)装置C中盛放烧碱溶液,目的是吸收反应后剩余的气体,防止污染空气.在该反应中,Cl元素的化合价既有升高又有降低,即在反应中Cl元素的原子既能获得电子也能失去电子,能否说氯元素既具有金属性又具有非金属性?简述你的理由.
不能
不能
金属性强弱的判断以元素的单质与水(或酸)反应置换氢的难易程度,以及它的最高价氧化物的水化物的碱性强弱为依据.非金属性的强弱以它与氢气生成氢化物的稳定性或它的最高价氧化物的水化物的酸性强弱来判断.(其他合理答案均可)
金属性强弱的判断以元素的单质与水(或酸)反应置换氢的难易程度,以及它的最高价氧化物的水化物的碱性强弱为依据.非金属性的强弱以它与氢气生成氢化物的稳定性或它的最高价氧化物的水化物的酸性强弱来判断.(其他合理答案均可)
.