网址:http://m.1010jiajiao.com/timu3_id_188108[举报]
下列说法中正确的是
A.冷的浓硫酸和浓硝酸都不可以用铝、铁的容器盛装
B.所有铵盐都易溶于水,所有铵盐中的氮均呈-3价
C.由于铵盐易和碱反应生成氨气,所以在实验室中一般用NH4Cl和NaOH的混合物制取氨气
D.金和铂不溶于浓硫酸和浓硝酸,但能溶于王水
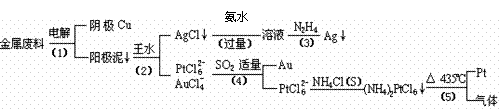
查看习题详情和答案>>(10分)从含银、锌、金和铂的金属铜废料中提取金、银、铂的一种工艺如下:高考资源网
(王水:浓硝酸与浓盐酸的混合物)高考资源网
 高考资源网
高考资源网
高考资
根据以上工艺回答下列问题:
(1)电解时,以铜金属废料为阳极,纯铜为阴极,CuSO4溶液为电解液,写出阳极电极反应方程式: 。
(2)肼(N2H4)是火箭发射常用的一种液体燃料,其完全燃烧时生成两种无污染的气体。已知部分共价键的键能数据如下表:
化学键 | N-N | O=O | N≡N | O-H | N-H |
键能/kJ?mol-1 | 193 | 499 | 941 | 460 | 393 |
则肼完全燃烧时的热化学方程式为: ;
(3)写出步骤(4)的离子反应方程式: ;
(4)金和浓硝酸反应的化学方程式为:Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O。但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释原因: 。
(5)已知室温下(NH4)2PtCl6的Ksp约为9×10-6。步骤(4)所得溶液中PtCl62-浓度为1×10-4mol?L- 1,则要从1 m3的该溶液中开始析出(NH4)2PtCl6沉淀至少需加入NH4Cl固体的质量为 kg。(设溶液体积的变化忽略不计)
查看习题详情和答案>>从含银、铜、金和铂的金属废料中提取金、银、铂的一种工艺如下:
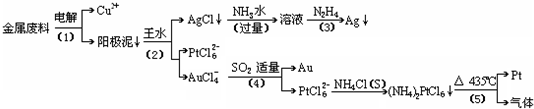
根据以上工艺回答下列问题:
(1)电解时,以______为阳极,纯铜为阴极,CuSO4溶液为电解液,则阳极的电极反应式为:______
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:______;
(3)写出步骤(4)的离子反应方程式:______;
(4)王水是______的混合液,其体积比为:______
(5)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:______.
查看习题详情和答案>>
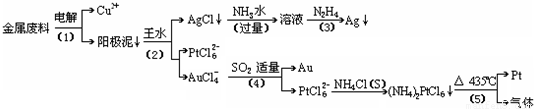
根据以上工艺回答下列问题:
(1)电解时,以______为阳极,纯铜为阴极,CuSO4溶液为电解液,则阳极的电极反应式为:______
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:______;
(3)写出步骤(4)的离子反应方程式:______;
(4)王水是______的混合液,其体积比为:______
(5)金和浓硝酸反应的化学方程式为:Au+6HNO3(浓)=Au(NO3)3+3NO2↑+3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之:______.
查看习题详情和答案>>
从含铜、银、金和铂的块状金属废料中提取铂、金、银的一种工艺如下:
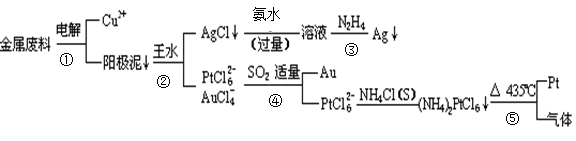
根据以上工艺回答下列问题:
(1)电解时,以_____________为阳极,纯铜为阴极,CuSO4溶液为电解液,则阴极的电极反应方程式为
(2)AgCl溶于氨水后所得的溶液含有的一种阳离子,在碱性条件下,也可用葡萄糖将其还原为银,写出该反应的离子方程式:
(3)写出步骤④的离子方程式:
(4)金和浓硝酸反应的化学方程式为:Au +6HNO3(浓)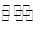 Au(NO3)3+3NO2↑+ 3H2O,因该反应正向进行的程度极小,所以金几乎不溶于浓硝酸,但金却可以溶于王水,试简要解释之:
Au(NO3)3+3NO2↑+ 3H2O,因该反应正向进行的程度极小,所以金几乎不溶于浓硝酸,但金却可以溶于王水,试简要解释之:
(5)写出反应⑤的化学反应方程式
____________________________________________________________________________
查看习题详情和答案>>