摘要:10,2.Na2CO3,Na2CO3.HCl(2)HCl+NaOH=NaCl+H2O, 2HCl+ Ca(OH)2=CaCl2+2H2O (3)NaOH.Na2CO3
网址:http://m.1010jiajiao.com/timu3_id_18767[举报]
某课外活动小组从海边盐滩上获得了一定量的粗盐,欲进行粗盐提纯的探究活动.请你参与其中,完成探究活动中的有关问题.
(1)查阅资料
①粗盐中含有较多的可溶性杂质(MgCl2、CaCl2等)和不溶性杂质(泥沙等).
②氯化钠在室温(20℃)时的溶解度为36.0g.
③Mg2+、Ca2+的碱和盐的溶解性(20℃)如下表:
说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水.
(2)实验方案设计与问题讨论
①溶解(20℃)用托盘天平称取10.0g粗盐,用药匙将该粗盐逐渐加入到盛有10mL水的烧杯里,边加边搅拌,直到粗盐不再溶解为止.此时加入的粗盐质量至少是 g.
②除杂若要除去粗盐中的可溶性杂质CaCl2,可向其中加入过量的Na2CO3溶液;若要除去杂质MgCl2,可向其中加入过量的 溶液,然后按右图所示装置进行 操作.再向滤液中加入适量的 即得到氯化钠溶液.如果观察所得滤液是浑浊的,再过滤,仍浑浊,其可能的原因是: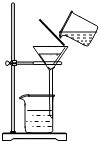 .
.
③蒸发
(3)实践实验操作过程略. 查看习题详情和答案>>
(1)查阅资料
①粗盐中含有较多的可溶性杂质(MgCl2、CaCl2等)和不溶性杂质(泥沙等).
②氯化钠在室温(20℃)时的溶解度为36.0g.
③Mg2+、Ca2+的碱和盐的溶解性(20℃)如下表:
| 阳离子\阴离子 | OH- | NO3- | SO42- | CO32- |
| Mg2+ | 不 | 溶 | 溶 | 微 |
| Ca2+ | 微 | 溶 | 微 | 不 |
(2)实验方案设计与问题讨论
①溶解(20℃)用托盘天平称取10.0g粗盐,用药匙将该粗盐逐渐加入到盛有10mL水的烧杯里,边加边搅拌,直到粗盐不再溶解为止.此时加入的粗盐质量至少是
②除杂若要除去粗盐中的可溶性杂质CaCl2,可向其中加入过量的Na2CO3溶液;若要除去杂质MgCl2,可向其中加入过量的

③蒸发
(3)实践实验操作过程略. 查看习题详情和答案>>
下表是一些粒子的半径(单位:10-10 m)
由其中数据可以看出:
(1)核电荷数相同的单原子核离子的大小顺序的规律性是什么?
(2)相同电子数且各层电子排布相同的离子,半径大小顺序的规律性是什么?
查看习题详情和答案>>
| 微粒 | O2- | F- | Na+ | M2+ | Al3+ | S2- | Cl- | Cl5+ | Cl7+ | K+ | Ca2+ |
| 半径 | 140 | 1.36 | 0.95 | 0.65 | 0.50 | 1.84 | 1.81 | 0.34 | 0.26 | 1.33 | 0.99 |
(1)核电荷数相同的单原子核离子的大小顺序的规律性是什么?
(2)相同电子数且各层电子排布相同的离子,半径大小顺序的规律性是什么?
27、小华在吃黄花鱼时,看到其头骨上有两块白色的小石头.[提出问题]这白色小石头中含有什么物质?
[查阅资料]小石头被称为“鱼脑石”,用来控制鱼在水中的沉浮.
[猜想与假设]如图

[供选试剂]10%稀盐酸,澄清石灰水,10%氢氧化钠溶液,紫色石蕊试液,酚酞试液.
[进行实验]验证小力的猜想.
[反思]如果实验证明了小力的猜想是正确的,你认为“鱼脑石”中一定含碳酸钙吗?简述理由.
查看习题详情和答案>>
[查阅资料]小石头被称为“鱼脑石”,用来控制鱼在水中的沉浮.
[猜想与假设]如图

[供选试剂]10%稀盐酸,澄清石灰水,10%氢氧化钠溶液,紫色石蕊试液,酚酞试液.
[进行实验]验证小力的猜想.
| 实验方法 | 可能看到的现象 | 结 论 |
| 1取粉碎后的“鱼脑石”加入 稀盐酸 ② 将生成的气体通入澄清石灰水 |
① 有气泡生成 ② 澄清石灰水变浑浊 |
小力的猜想是正确的(“鱼脑石”中含有CO32-) |
不能
,上述实验只证明“鱼脑石”中CO32-的存在,没有证明Ca2+的存在(或含有碳酸根离子的化合物不一定就是碳酸钙)
.10、以下是部分盐的溶解性表(20℃)
|
查看习题详情和答案>>
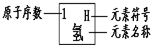 19、元素周期律是学习和研究化学的重要工具.下表是元素周期表的部分信息:
19、元素周期律是学习和研究化学的重要工具.下表是元素周期表的部分信息:| 1 H 氢 |
2 He 氦 | ||||||
| 3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
| 11 Na 钠 |
12 Mg 镁 |
13 A1 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
X C1 氯 |
18 Ar 氩 |
| 19 K 钾 |
20 Ca 钙 |
… | |||||
非金属
(填‘金属’或‘非金属’),它在化学反应中容易得
(填‘得’或‘失’)电子.(2)元素的化学性质与原子结构中的
最外层电子
数关系密切.(3)地壳中含量最多的元素的原子序数是
8
.(4)分析上表规律,可推知,表中X=
17
.(5)
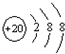 表示的是(写粒子符号)
表示的是(写粒子符号)Ca2+
.