摘要:21.某同学通过查阅资料得知.铝热反应所得到的熔融物应该是铁铝合金. (1)设计一个最简单的实验方案.证明上述所得的块状熔融物中含有金属铝.写出表示该实验原理的离子方程式: . (2)某同学取一定量上述的熔融物与过量的.且很稀的硝酸充分反应.发现反应过程中无气体放出.在反应结束后的溶液中.逐滴加入4mo1·L-1的氢氧化钠溶液.所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示.在AB段.有刺激性气味的气体产生. 试回答下列问题: ①熔融物与稀硝酸充分反应后.还原产物NH4NO3的物质的量为 . ②熔融物中金属铝的物质的量为 ,金属铁的物质的量为 .
网址:http://m.1010jiajiao.com/timu3_id_184873[举报]
(8分)某同学通过查阅资料得知,铝热反应所得到的熔融物应该是铁铝合金。
(1)设计一个最简单的实验方案,证明上述所得的块状熔融物中含有金属铝。写出表示该实验原理的离子方程式: 。
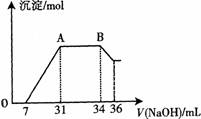 (2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1?L―1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
(2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1?L―1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为 。
②熔融物中金属铝的物质的量为 ;金属铁的物质的量为 。
查看习题详情和答案>>(8分)某同学通过查阅资料得知,铝热反应所得到的熔融物应该是铁铝合金。
(1)设计一个最简单的实验方案,证明上述所得的块状熔融物中含有金属铝。写出表示该实验原理的离子方程式: 。
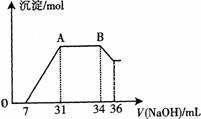 (2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
(2)某同学取一定量上述的熔融物与过量的、且很稀的硝酸充分反应,发现反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mo1·L—1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mo1)的关系如图所示。在AB段,有刺激性气味的气体产生。
试回答下列问题:
①熔融物与稀硝酸充分反应后,还原产物NH4NO3的物质的量为 。
②熔融物中金属铝的物质的量为 ;金属铁的物质的量为 。
查看习题详情和答案>>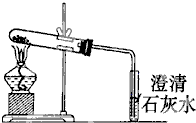 镁将成为21世纪重要的轻型环保材料.
镁将成为21世纪重要的轻型环保材料.(1)海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中MgCl2
| 熟石灰 |
| 过滤 |
| 盐酸 |
| 蒸发、浓缩、结晶 |
| 脱水 |
| 通电 |
①在实验室进行过滤操作时需要用到玻璃棒,其作用是
引流
引流
.②电解熔融氯化镁的过程中,
电
电
能转化为化学
化学
能.(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧.燃烧的化学方程式为
2Mg+CO2=C+2MgO,此反应类型属于
C
C
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为-3.据此写出氮化镁的化学式
Mg3N2
Mg3N2
.(3)镁铝合金广泛用于火箭、导弹和飞机制造业等.某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.0 |
1:3
1:3
.所用氢氧化钠溶液的溶质质量分数为40%
40%
.(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属.但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是Mg2(OH)2CO3;小花认为可能是Mg(OH)2.小赵认为小明的猜想是错误的,其理由是
氧化镁为白色固体与水缓慢反应生成氢氧化镁
氧化镁为白色固体与水缓慢反应生成氢氧化镁
.实验探究:小赵按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体.
实验分析:实验后,小赵认为小花的猜想也是错误的,其理由是
样品分解生成的二氧化碳使澄清石灰水变浑浊
样品分解生成的二氧化碳使澄清石灰水变浑浊
.查阅资料得出结论:Mg(OH)2 和 Mg2(OH)2CO3 都可以加热分解,产物均为氧化物,据此请你写出Mg2(OH)2CO3 加热
分解的化学方程式
Mg2(OH)2CO3
2MgO+CO2↑+H2O
| ||
Mg2(OH)2CO3
2MgO+CO2↑+H2O
.
| ||