摘要:24.为测定标示质量分数为32%的盐酸(图1)的实际质量分数.小明用pH测定仪组成实验装置(图2).实验时先在烧杯中加入20 g 40%的氢氧化钠溶液.再逐滴加人该盐酸.测定仪打印出加入盐酸的质量与烧杯中溶液pH的关系图(图3).发生反应的化学方程式为: NaOH+HCl=NaCl+H20 (1)请以此次测定的结果.列式计算该盐酸的实际质量分数, (2)请分析你的计算结果与标签标示的质量分数不一致的可能原因.
网址:http://m.1010jiajiao.com/timu3_id_18413[举报]
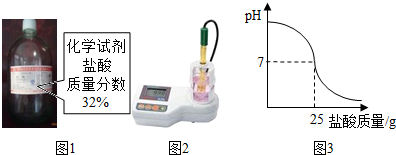
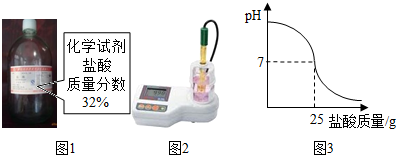
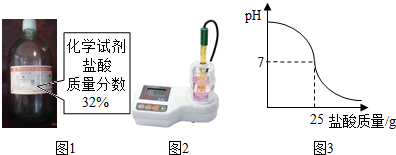
为测定标示质量分数为32%的盐酸(图1)的实际质量分数,小明用pH测定仪组成实验装置(图2).实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定仪打印出加入盐酸的质量与烧杯中溶液pH的关系图(图3).
(1)请以此次测定的结果,计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因.
(3)另取50g该盐酸于一大烧杯中,加入58.8g某浓度的碳酸钠溶液恰好完全反应,求烧杯中所得溶液的溶质质量分数. 查看习题详情和答案>>

(1)请以此次测定的结果,计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因.
(3)另取50g该盐酸于一大烧杯中,加入58.8g某浓度的碳酸钠溶液恰好完全反应,求烧杯中所得溶液的溶质质量分数. 查看习题详情和答案>>
为测定标示质量分数为32%的盐酸(图1)的实际质量分数,小明用pH测定仪组成实验装置(图2).实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,测定仪打印出加入盐酸的质量与烧杯中溶液pH的关系图(图3).发生反应的化学方程式为:NaOH+HCl=NaCl+H20.

(1)请以此次测定的结果,列式计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因. 查看习题详情和答案>>

(1)请以此次测定的结果,列式计算该盐酸的实际质量分数;
(2)请分析你的计算结果与标签标示的质量分数不一致的可能原因. 查看习题详情和答案>>