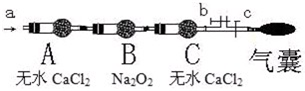
摘要:21.高一教材中有一演示实验.用脱脂棉包住约0.2g过氧化钠粉末.置于石棉网上.往脱脂棉上滴水.观察到脱脂棉 剧烈燃烧起来. (1) 由上述实验现象所得出的有关过氧化钠跟水 反应的结论是:a:有氧气生成.b: . (2) 写出Na2O2和H2O反应的化学方程式并标出 电子转移的方向与数目: . 其中还原剂是 .氧化剂是 . (3)某研究性学习小组拟用A图所示装置进行实验.以证明上述结论.用以验证第一条结论的实验方法 用以验证第二条结论的实验方法是: 22.右图是加热分解碳酸氢钠的实验装置图. (1)盛澄清石灰水的试管中可观察到的现象 是 有关反应的离子方程式 (2)盛澄清石灰水的试管中不再出现气泡时. 停止实验的正确操作是 (3)证明试验中碳酸氢钠已完全分解的方法是 (4)实验结束时发现盛澄清石灰水的试管中又重新变成透明澄清的溶液.写出其中发生反应的离子方程式
网址:http://m.1010jiajiao.com/timu3_id_174406[举报]
高一教材中的一个演示实验:用脱脂棉包住0.2gNa2O2粉末,放在石棉网上,在脱脂棉上滴加几滴水;可以观察到脱脂棉剧烈燃烧起来。此实验现象说明:
A.Na2O2与H2O反应是一个放热反应 B.Na2O2与H2O反应中有氧气生成
C.Na2O2与H2O反应中有氢氧化钠生成 D.Na2O2与H2O反应中有中间产物H2O2生成
查看习题详情和答案>>
高一教材中演示钠与水的反应是进行了两次实验:第一次实验在烧杯中进行,观察钠与水反应的现象;第二次实验在塑料瓶中进行,用于收集、检验反应生成的气体。
第一次实验中,钠球在水面上游动,其原因是_______________;第二次实验中,实验前先要将塑料瓶挤瘪,这样做的目的是___________________。
查看习题详情和答案>>
第一次实验中,钠球在水面上游动,其原因是_______________;第二次实验中,实验前先要将塑料瓶挤瘪,这样做的目的是___________________。
查看习题详情和答案>>
(08广东实验中学三模)高一教材中的一个演示实验:用脱脂棉包住0.2gNa2O2粉末,放在石棉网上,在脱脂棉上滴加几滴水;英才苑可以观察到脱脂棉剧烈燃烧起来。此实验现象说明()
A.Na2O2与H2O反应是一个放热反应
B.Na2O2与H2O反应中有氧气生成
C.Na2O2与H2O反应中有氢氧化钠生成
D.Na2O2与H2O反应中有中间产物H2O2生成
查看习题详情和答案>>高一教材中的一个演示实验:用脱脂棉包住0.2gNa2O2粉末,放在石棉网上,在脱脂棉上滴加几滴水;可以观察到脱脂棉剧烈燃烧起来。此实验现象说明:
- A.Na2O2与H2O反应是一个放热反应
- B.Na2O2与H2O反应中有氧气生成
- C.Na2O2与H2O反应中有氢氧化钠生成
- D.Na2O2与H2O反应中有中间产物H2O2生成