摘要:32.根据下列变化关系.请回答下列问题: (1)写出A物质的名称 .加B溶液的作用为 . (2)写出④.⑥两步反应的化学方程式.并在( )号中标明反应类型. ④ , ⑥ . 高一年级化学第二学期期末模拟检测试题 座位号
网址:http://m.1010jiajiao.com/timu3_id_173096[举报]
根据下列变化关系,请回答下列问题:

(1)写出A物质的名称____________。加B溶液的作用为__________________。
(2)写出④、⑥两步反应的化学方程式,并在( )号中标明反应类型。
④_______________( );
⑥_______________( )。
查看习题详情和答案>>
(2)写出④、⑥两步反应的化学方程式,并在( )号中标明反应类型。
④_______________( );
⑥_______________( )。
根据下列变化关系,请回答下列问题:
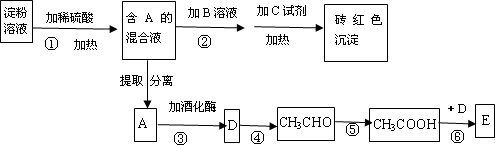
(1)写出A物质的名称________.加B溶液的作用为________.
(2)写出④、⑥两步反应的化学方程式,并在( )号中标明反应类型.
④________( );
⑥________( );
根据下列框图回答问题:
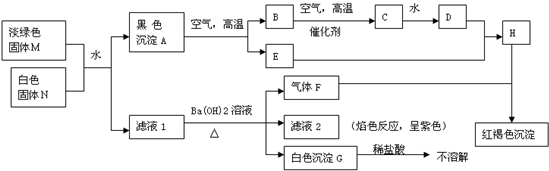
已知白色固体N中阴、阳离子具有相同的核外电子层结构.
(1)请写出M与N反应的离子方程式:______.
(2)写出由A在空气中锻烧的化学方程式______.
(3)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子.请写出上述变化过程中的离子方程式______.
(4)类似上述框图中A、B、C之间的转化关系一般可以表示为(副产物已略去):
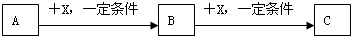
则下列说法正确的是______
a.若A是非金属单质,则C与水反应的生成物可能是强酸或弱酸
b.若A是金属单质,则C与水反应的生成物可能是强碱
c.若A是化合物,则C与水反应的生成物可能是强酸
d.若X是强碱,则C可能是正盐或酸式盐.
查看习题详情和答案>>
下列图1中A是常见的金属,B是一种常见的无色无味的液体.C是一种有磁性的黑色氧化物,E是一种无色无味的有毒气体.根据下列图1、图2,回答下列问题:

(1)写出A+B的蒸气高温反应的化学方程式:
(2)E和N2是等电子体,电子式相似,请写出E可能的电子式:

(3)在101kPa和150℃时,可逆反应E (g)+B (g) F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
A、升高温度B、增大压强C、加入催化剂
(4)若G是一种黄绿色单质气体,则H的水溶液呈
查看习题详情和答案>>

(1)写出A+B的蒸气高温反应的化学方程式:
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
| ||
(2)E和N2是等电子体,电子式相似,请写出E可能的电子式:


(3)在101kPa和150℃时,可逆反应E (g)+B (g)
 F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)
F (g)+D (g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母)BC
BC
.A、升高温度B、增大压强C、加入催化剂
(4)若G是一种黄绿色单质气体,则H的水溶液呈
酸
酸
性(填“酸、碱、中”),理由是(用离子反应方程式表示):Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
.若向0.01mol?L-1 10ml H的溶液中加入等体积等浓度的KSCN溶液,现象黄色溶液变为红色
黄色溶液变为红色
.向该混合体系中加入少量1mol?L-1 KSCN溶液,溶液颜色变深
变深
,若改加少量KCl浓溶液颜色不变
不变
(填“变深、变浅、不变”).下列图1中B是一种常见的无色无味的液体。C是一种有磁性的化合物,E是一种无色无味的有毒气体。根据下列图1、图2,回答下列问题:
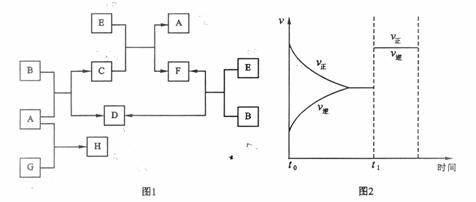
(1)写出C的化学式: 。
(2)E和N2是等电子体,请写出可能E的电子式:
(3)在101kPa和150℃时,可逆反应E(g) + B(g)![]() F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
F(g) + D(g)反应速率和时间的关系如图2所示,那么在t1时速率发生改变的原因可能是(填选项字母) 。
A.升高温度 B.增大压强 C.加入催化剂
(4)若G是一种淡黄色固体单质,16 g G和足量的A反应放出的热量为Q kJ(Q > 0),写出这个反应的热化学方程式: 。
若G是一种气态单质,H的水溶液可以和有机物I反应使溶液呈紫色,请写出I的结构简式: ;H的水溶液呈酸性,请用离子方程式表示呈酸性的原因:
查看习题详情和答案>>