网址:http://m.1010jiajiao.com/timu3_id_172170[举报]
一定温度和压强下N2+3H2![]() 2NH3反应达到平衡后,下列说法中正确的是
2NH3反应达到平衡后,下列说法中正确的是
A.N2与H2不再化合,NH3不再分解
B.N2、H2化合成氨的反应速率等于NH3 分解的反应速率
C.H2、NH3的体积分数相等
D.N2、H2、NH3的物质的量浓度相等
查看习题详情和答案>>氮气与氢气反应生成氨气的平衡常数见下表:
| | N2+3H2 2NH3 2NH3 | |||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
(1)工业上合成氨的温度一般控制在500℃,原因是 。
(2)在2 L密闭容器中加入1 mol氮气和3 mol氢气,进行工业合成氨的模拟实验,若2分钟后,容器内压强为原来的0.8倍,则0到2分钟,氨气的反应速率为________mol/(L·min)。
(3)下列说法能表明该反应达到平衡的是________
A.气体的平均分子量不再变化 B.密闭容器内的压强不再变化
C.v (N2) =" 2" v (NH3) D.气体的密度不再变化
(4)下列措施,既能加快该反应的反应速率,又能增大转化率的是______________
A.使用催化剂 B.缩小容器体积 C.提高反应温度 D.移走NH3
(5)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是______。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(6)将氨水与盐酸等浓度等体积混合,下列做法能使c(NH4+)与c(Cl-)比值变大的是________
A. 加入固体氯化铵 B.通入少量氯化氢
C. 降低溶液温度 D.加入少量固体氢氧化钠 查看习题详情和答案>>
| | N2+3H2 2NH3 2NH3 | |||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
(1)工业上合成氨的温度一般控制在500℃,原因是 。
(2)在2 L密闭容器中加入1 mol氮气和3 mol氢气,进行工业合成氨的模拟实验,若2分钟后,容器内压强为原来的0.8倍,则0到2分钟,氨气的反应速率为________mol/(L·min)。
(3)下列说法能表明该反应达到平衡的是________
A.气体的平均分子量不再变化 B.密闭容器内的压强不再变化
C.v (N2) =" 2" v (NH3) D.气体的密度不再变化
(4)下列措施,既能加快该反应的反应速率,又能增大转化率的是______________
A.使用催化剂 B.缩小容器体积 C.提高反应温度 D.移走NH3
(5)常温下,在氨水中加入一定量的氯化铵晶体,下列说法错误的是______。
A.溶液的pH增大 B.氨水的电离度减小 C.c(OH-)减小 D.c(NH4+)减小
(6)将氨水与盐酸等浓度等体积混合,下列做法能使c(NH4+)与c(Cl-)比值变大的是________
A. 加入固体氯化铵 B.通入少量氯化氢
C. 降低溶液温度 D.加入少量固体氢氧化钠
(10分)已知:合成氨反应为N2+3H2![]() 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系 (填“I”“II”“III”)
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为 (填“A”“B”“C”“D”)
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =
查看习题详情和答案>>
(10分)已知:合成氨反应为N2+3H2 2NH3(正反应为放热反应),分析下列问题:
2NH3(正反应为放热反应),分析下列问题:
(1)在一定温度时,可用图中哪一条曲线表示反应物的转化率和压强之间的关系 (填“I”“II”“III”)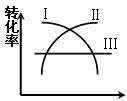
(2)在不同温度和压强下(P1>P2),合成氨反应达到平衡时,混合气体中氨气的体积分数Z%
随温度变化的曲线应为 (填“A”“B”“C”“D”)
(3)将N2和H2按1:3的体积比通入合成塔,反应达平衡后,NH3的体积分数为20%,则达到平衡时,N2和H2的转化率之比α(N2)∶α (H2)= ;平衡时N2的转化率为_________;平衡混合气体中,n(N2)∶n(H2)∶n(NH3) =