摘要:21.现有K2CO3.AgNO3和Ba(OH)2三种无色溶液.选用一种试剂把它们鉴别出来.这种试剂可选用 .有关化学反应方程式是: , , .
网址:http://m.1010jiajiao.com/timu3_id_171459[举报]
现有失去标签的四瓶无色溶液A、B、C、D,只知道它们是K2CO3、K2SO4、H2SO4和Ba(NO3)2,为了鉴别它们,进行如下实验:
①A+D-→溶液+气体 ②B+C-→溶液+沉淀
③B+D-→溶液+沉淀 ④A+B-→溶液+沉淀
⑤将④得到的沉淀物加入③所得溶液中,④中沉淀很快溶解并产生无色无味的气味.
根据以上实验事实,请回答如下问题:
(1)A、B、C、D四种无色溶液分别为
(2)写出下列各步反应的离子方程式
①
查看习题详情和答案>>
①A+D-→溶液+气体 ②B+C-→溶液+沉淀
③B+D-→溶液+沉淀 ④A+B-→溶液+沉淀
⑤将④得到的沉淀物加入③所得溶液中,④中沉淀很快溶解并产生无色无味的气味.
根据以上实验事实,请回答如下问题:
(1)A、B、C、D四种无色溶液分别为
K2CO3
K2CO3
、Ba(NO3)2
Ba(NO3)2
、K2SO4
K2SO4
、H2SO4
H2SO4
(用化学式表示)(2)写出下列各步反应的离子方程式
①
2H++CO32-=CO2↑+H2O
2H++CO32-=CO2↑+H2O
②Ba2++SO42-=BaSO4↓
Ba2++SO42-=BaSO4↓
⑤BaCO3+2H+=Ba2++CO2↑+H2O
BaCO3+2H+=Ba2++CO2↑+H2O
.
现有失去标签的四瓶无色溶液A、B、C、D,只知道它们是K2CO3、K2SO4、H2SO4和Ba(NO3)2,为了鉴别它们,进行如下实验:
①A+D-→溶液+气体②B+C-→溶液+沉淀③B+D-→溶液+沉淀④A+B-→溶液+沉淀
将④得到的沉淀物加入③所得溶液中,④中沉淀很快溶解并产生无色无味的气味.
(1)根据以上实验事实,A、C、D三种无色溶液分别为 、 、 (用化学式表示).
(2)写出①②中发生反应的离子方程式:① ;② .
(3)离子反应是中学化学中重要的反应类型,在发生离子反应的反应物或生成物中,一定存在有
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物. 查看习题详情和答案>>
①A+D-→溶液+气体②B+C-→溶液+沉淀③B+D-→溶液+沉淀④A+B-→溶液+沉淀
将④得到的沉淀物加入③所得溶液中,④中沉淀很快溶解并产生无色无味的气味.
(1)根据以上实验事实,A、C、D三种无色溶液分别为
(2)写出①②中发生反应的离子方程式:①
(3)离子反应是中学化学中重要的反应类型,在发生离子反应的反应物或生成物中,一定存在有
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物. 查看习题详情和答案>>
现有失去标签的四瓶无色溶液A、B、C、D,只知它们是K2CO3、K2SO4、NaHSO4和Ba(NO3)2,为鉴别它们,进行如下实验:
①A+D→溶液+气体②B+C→溶液+沉淀
③B+D→溶液+沉淀④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,④中沉淀很快溶解并产生无色无味的气体.
根据以上实验事实,请回答下列问题:
(1)A、C两种无色溶液分别为:
(2)下列各步反应的离子方程式依次为:
①
②
⑤
查看习题详情和答案>>
①A+D→溶液+气体②B+C→溶液+沉淀
③B+D→溶液+沉淀④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,④中沉淀很快溶解并产生无色无味的气体.
根据以上实验事实,请回答下列问题:
(1)A、C两种无色溶液分别为:
K2CO3
K2CO3
、K2SO4
K2SO4
. (用化学式表示)(2)下列各步反应的离子方程式依次为:
①
2H++CO32-═CO2↑+H2O
2H++CO32-═CO2↑+H2O
②
Ba2++SO42-═BaSO4↓
Ba2++SO42-═BaSO4↓
⑤
BaCO3+2H+═Ba2++CO2↑+H2O
BaCO3+2H+═Ba2++CO2↑+H2O
.某盐卤矿抽出的废液中含有大量的K+、Cl-、Br-,及少量的Ca2+、Mg2+、SO42-.某研究性学习小组拟取该废液来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
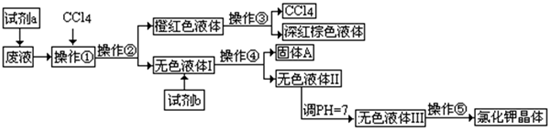
现有可供选择的a、b试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3.请根据以上流程,回答相关问题:
(1)试剂a应选
(2)操作①、②、③、④、⑤的名称依次为
A.萃取、过滤、分液、过滤、蒸发结晶 B.萃取、分液、分液、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶 D.萃取、分液、蒸馏、过滤、蒸发结晶
(3)操作⑤中用到的瓷质仪器名称是
(4)选出除去无色液体I中Ca2+、Mg2+、SO42-离子所需的试剂,按滴加顺序依次为
(5)调节pH的作用是
查看习题详情和答案>>

现有可供选择的a、b试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2、KMnO4(H+)溶液、稀HNO3.请根据以上流程,回答相关问题:
(1)试剂a应选
H2O2
H2O2
,该反应在酸性环境中完成,其离子方程式为H2O2;H2O2+2Br-+2H+=Br2+2H2O
H2O2;H2O2+2Br-+2H+=Br2+2H2O
.(2)操作①、②、③、④、⑤的名称依次为
D
D
(选填字母).A.萃取、过滤、分液、过滤、蒸发结晶 B.萃取、分液、分液、过滤、蒸发结晶
C.分液、萃取、过滤、过滤、蒸发结晶 D.萃取、分液、蒸馏、过滤、蒸发结晶
(3)操作⑤中用到的瓷质仪器名称是
蒸发皿
蒸发皿
.(4)选出除去无色液体I中Ca2+、Mg2+、SO42-离子所需的试剂,按滴加顺序依次为
BaCl2、KOH、K2CO3
BaCl2、KOH、K2CO3
(填化学式).(5)调节pH的作用是
除去过量的OH-、CO32-
除去过量的OH-、CO32-
.实验室需要制备纯净的氯化钾.现有含少量KBr和K2SO4的氯化钾样品,按照下图所示的实验方案进行提纯.
(1)检验加入BaCl2溶液后S042-是否沉淀完全的操作为
(2)若用硝酸钡来代替氯化钡,请判断是否可行,并说明理由:
(3)某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液他的思路如下,请写出方框内或横线①②③④⑤中溶质或沉淀(或物质)的化学式:

查看习题详情和答案>>

(1)检验加入BaCl2溶液后S042-是否沉淀完全的操作为
静置一段时间后.取少量上层澄清溶液再漓加BaCl2溶液,若无沉淀生成,说明SO42-沉淀完全,反之未沉淀完全
静置一段时间后.取少量上层澄清溶液再漓加BaCl2溶液,若无沉淀生成,说明SO42-沉淀完全,反之未沉淀完全
;(2)若用硝酸钡来代替氯化钡,请判断是否可行,并说明理由:
否,会引入硝酸钾杂质
否,会引入硝酸钾杂质
;(3)某同学认为该实验方案中加适量氯化钡溶液不容易控制,应加入过量氯化钡溶液他的思路如下,请写出方框内或横线①②③④⑤中溶质或沉淀(或物质)的化学式:
①KCI.KBr.BaCl2②K2CO3③BaCO3④KCI.KBr.K2CO3⑤HCL和Cl2
①KCI.KBr.BaCl2②K2CO3③BaCO3④KCI.KBr.K2CO3⑤HCL和Cl2
.