摘要:26.(未标分数的每格1分.本题共12分) (1)补进气管升入近集气瓶底 (2)① Cu + 2H2SO4(浓) CuSO4 + SO2↑+ 2H2O . m/64 . 还原 . m/32 ②D ③稀硫酸不与铜反应 (3)方案一:产生的气体中含有水蒸气.干燥管中的质量差不仅仅是SO2的质量(或烧瓶中的二氧化硫不能完全排出)方案二:沉淀的质量一部分是高锰酸钾溶液中起酸化作用的硫酸与氯化钡反应而产生的 方案三: V/ mol/L
网址:http://m.1010jiajiao.com/timu3_id_171382[举报]
(2007?资阳二模)某学生用如图所示装置制取氯气,并收集氯气进行实验.清回答下列问题: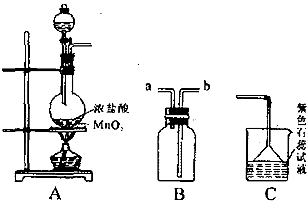
(1)装置A发生反应的离子方程式为
(2)装置 B 如图所示放置,则连接 A 的导管口是(填管口字母)
(3)实验中可观察到C 处石蕊试液的现象是
(4)取出 B 中的集气瓶进行氯气与铜的燃烧实验:首先进行的操作是
(5〕Cl2可与甲苯在光照条件下反应生成一氯甲苯,一氯甲苯进一步水解,可得某种香精的原料苯甲醇.为了获得较纯的一氯甲苯,同时回收未反应的甲苯应采用
A.分液漏斗 B.酒精灯 C.铁架台 D.蒸馏烧瓶 E.短颈漏斗 F.水冷凝管
G.玻璃捧 H.温度计 I.尾接管 J.烧杯 K.锥形瓶.
查看习题详情和答案>>

(1)装置A发生反应的离子方程式为
MnO2+4H++2C1-
Mn2++C12↑+2H2O
| ||
MnO2+4H++2C1-
Mn2++C12↑+2H2O
| ||
(2)装置 B 如图所示放置,则连接 A 的导管口是(填管口字母)
b
b
;(3)实验中可观察到C 处石蕊试液的现象是
先变红后褪色
先变红后褪色
,其原因是C中生成的氯化氢溶液使石蕊变红色,生成的次氯酸具有漂白性使红色褪去
C中生成的氯化氢溶液使石蕊变红色,生成的次氯酸具有漂白性使红色褪去
;(4)取出 B 中的集气瓶进行氯气与铜的燃烧实验:首先进行的操作是
用坩埚钳夹住一束铜丝灼烧
用坩埚钳夹住一束铜丝灼烧
,然后立刻放入充满氯气的集气瓶中;实验过程中有同学提出应该在集气瓶底先放少量的水或细沙,你认为不需要
不需要
(填“需要”或“不需要”),理由是实验过程中生成的是棕黄色烟,不是温度较高的固体熔融物,不会炸裂瓶底
实验过程中生成的是棕黄色烟,不是温度较高的固体熔融物,不会炸裂瓶底
;(5〕Cl2可与甲苯在光照条件下反应生成一氯甲苯,一氯甲苯进一步水解,可得某种香精的原料苯甲醇.为了获得较纯的一氯甲苯,同时回收未反应的甲苯应采用
分馏
分馏
方法将其分离,在分离时需要的玻璃仪器有BDFHIK
BDFHIK
(填序号).A.分液漏斗 B.酒精灯 C.铁架台 D.蒸馏烧瓶 E.短颈漏斗 F.水冷凝管
G.玻璃捧 H.温度计 I.尾接管 J.烧杯 K.锥形瓶.
某校实验小组进行实验研究(实验装置示意图如下).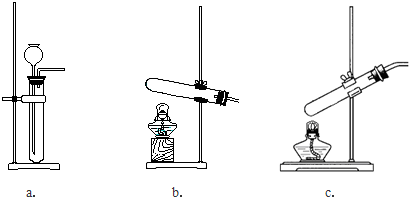
(1)制取氧气可选用的发生装置是
(2)①该小组用装置b制得NH3.其反应的化学方程式为
②该小组用装置b进行铁和水蒸气的反应,其化学方程式为
(3)该小组用装置c可进行的实验有
查看习题详情和答案>>

(1)制取氧气可选用的发生装置是
ab
ab
(填字母序号).该小组用制取的氧气进行硫在氧气中燃烧的性质实验时,在集气瓶底加入了少量氢氧化钠溶液.盛放该溶液的目的是充分吸收生成的二氧化硫,减少污染空气
充分吸收生成的二氧化硫,减少污染空气
.(2)①该小组用装置b制得NH3.其反应的化学方程式为
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑
.②该小组用装置b进行铁和水蒸气的反应,其化学方程式为
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(3)该小组用装置c可进行的实验有
浓硫酸和铜反应
浓硫酸和铜反应
(写出一个即可).下列实验室制取气体的操作中,错误的是( )
| A、导气管口刚有气泡冒出时,立即收集气体 | B、用排水法收集难溶于水的气体 | C、用敞开体系排空气法收集气体时,导气管应伸进集气瓶的底部 | D、某气体的密度比空气小,盛满该气体的集气瓶应倒放在桌面上 |