网址:http://m.1010jiajiao.com/timu3_id_169264[举报]
下图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
|
A |
|
C |
|
|
B |
|
A、三种元素的原子半径的大小顺序是:B>C>A
B、A元素最高价氧化物对应的水化物具有强氧化性
C、B元素的氧化物、氢化物的水溶液都呈酸性
D、C元素是非金属性最强的元素
【解析】考查元素周期表的结构和元素周期律的应用。因为质子数和中子数之和是质量数,若A的原子序数是x,则B是x+9,C是x+2。根据题意可知x+x+2+x+9=2×(x+9),解得x=7,则A、B、C分别是N、S、F。同主族元素自上而下原子半径逐渐增大,非金属性逐渐减弱,金属性逐渐增强。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强,金属性逐渐减弱。A不正确,应该是B>A>C,硝酸是氧化性酸,B正确。硫酸和氢硫酸都属于酸,C正确。F是最强的非金属元素,D正确,所以答案是A。
查看习题详情和答案>>
下图是周期表中短周期的一部分,A、B、C三种元素原子核外电子数之和等于B原子的质量数。B原子核内质子数和中子数相等。下列叙述不正确的是( )
| A |
| C |
|
| B |
|
A、三种元素的原子半径的大小顺序是:B>C>A
B、A元素最高价氧化物对应的水化物具有强氧化性
C、B元素的氧化物、氢化物的水溶液都呈酸性
D、C元素是非金属性最强的元素
【解析】考查元素周期表的结构和元素周期律的应用。因为质子数和中子数之和是质量数,若A的原子序数是x,则B是x+9,C是x+2。根据题意可知x+x+2+x+9=2×(x+9),解得x=7,则A、B、C分别是N、S、F。同主族元素自上而下原子半径逐渐增大,非金属性逐渐减弱,金属性逐渐增强。同周期元素自左向右原子半径逐渐减小,非金属性逐渐增强,金属性逐渐减弱。A不正确,应该是B>A>C,硝酸是氧化性酸,B正确。硫酸和氢硫酸都属于酸,C正确。F是最强的非金属元素,D正确,所以答案是A。
查看习题详情和答案>>
2- 4 |
①通入一定量Cl2后,加入CCl振荡,静置后CCl层呈紫红色,用分液漏斗分液;
②向分液后的水溶液中加入足量硝酸酸化的硝酸钡溶液,产生白色沉淀;
③过滤后将滤液分为两份,向一份中加入硝酸酸化的硝酸银溶液,产生大量沉淀,向另一份中加入少量KSCN溶液,溶液立即变为血红色.
根据上述实验,以下推测正确的是( )
| A、无法确定原溶液中是否存在Cl-、Na+? | ||
B、原溶液中肯定存在的离子有Fe3+、SO
| ||
| C、原溶液一定显中性 | ||
| D、原溶液中肯定不存在的离子有Fe2+、Br- |
A.有酸性和氧化性,无还原性
B.有酸性、氧化性和还原性
C.有酸性、还原性,无氧化性
D.盐酸是非氧化性酸,在化学反应中不可能表现氧化性
查看习题详情和答案>>已知CO2和SO2的化学性质具有相似性和差异性。
(1)写出CO2与 Na2O2反应的化学方程式___________________________。
(2)某学生判断SO2和Na2O2反应可能生成硫酸钠。
① 你认为他的判断合理吗? ,简要说明理由: 。
② 该同学为了确认SO2和Na2O2反应中是否有氧气生成吗,拟使用下列装置进行实验。
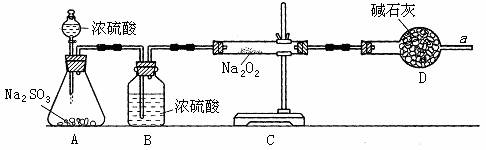
B装置的作用是 ;
D装置的作用是 。
③ 为确认SO2和Na2O2反应的产物,该同学设计了以下实验操作,你认为应该进行的操作(按先后顺序排列)是 (填序号)。
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧。
B.将C装置中反应后的固体物质溶于适量水配成溶液。
C.在配成的溶液中加入用硝酸(氧化性酸)酸化的硝酸钡溶液,观察是否有沉淀生成。
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成。
查看习题详情和答案>>