摘要:33.甲.乙.丙.丁为4种单质.其中甲.乙.丙为前三周期元素的单质.常温下均为气态,丁是日常生活中一种常见的金属.甲.乙.丙.丁分别点燃生成X.Y.Z.W 4种化合物的转化关系如下: 甲 + 丙 X 甲 + 丁 Y 丙 + 乙 Z 丁 + 乙 W 常温下X是无色液体.Y是黑色固体.丙在乙中燃烧发出苍白色火焰.丁在乙中燃烧生成 棕黄色的烟.W的水溶液呈黄色. 试回答: (1)已知丙和乙在反应过程中.破坏1mol丙单质中的化学键消耗的能量为Q1kJ.破坏1mol乙单质中的化学键消耗的能量Q2 kJ.破坏1mol Z中的化学键消耗的能量Q3 kJ.试比较Q1 + Q2 > Q3 ( 填“ < .“> 或“= ). (2)X的化学键类型为 共价键 .丙原子和乙原子结合形成分子趋势的原因为 丙原子最外层有1个电子.还缺少1个电子就达到了最外层2电子的稳定结构.而乙原子最外层有7个电子.也还缺少1个电子便达到了8电子稳定结构.所以两者共用一对电子对.彼此达到稳定结构. (3)写出丁加入到W溶液中反应的离子方程式 2Fe3+ + Fe == 3Fe2+ . (4)气体丙在甲中完全燃烧生成X的化学反应方程式为 2H2 + O2 == 2H2O
网址:http://m.1010jiajiao.com/timu3_id_167435[举报]
甲、乙、丙、丁为四种单质,其中两种为气体,且一种为黄绿色气体,A、B、C、D、E均为化合物,E常温下为无色液体,它们之间的转化关系如图所示:
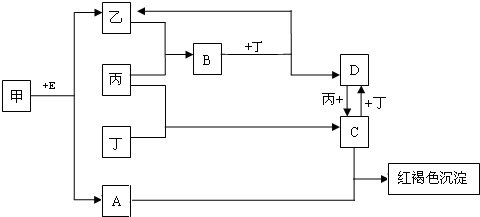
请回答下列问题
(1)写出下列物质的化学式:丁
(2)检验C溶液中所含阳离子的试剂是:
(3)丙与A溶液反应的离子方程式:
(4)C溶液与丁反应生成D的化学方程式:
查看习题详情和答案>>

请回答下列问题
(1)写出下列物质的化学式:丁
Fe
Fe
,DFeCl2
FeCl2
;(2)检验C溶液中所含阳离子的试剂是:
KSCN溶液
KSCN溶液
,现象:溶液出现血红色
溶液出现血红色
;(3)丙与A溶液反应的离子方程式:
Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
;(4)C溶液与丁反应生成D的化学方程式:
Fe+2FeCl3═3FeCl2
Fe+2FeCl3═3FeCl2
.甲、乙、丙、丁为四种单质,其中两种为气体,且一种为黄绿色气体,A、B、C、D、E均为化合物,E常温下为无色液体,它们之间的转化关系如图所示:

请回答下列问题
(1)写出下列物质的化学式:丁______,D______;
(2)检验C溶液中所含阳离子的试剂是:______,现象:______;
(3)丙与A溶液反应的离子方程式:______;
(4)C溶液与丁反应生成D的化学方程式:______.
查看习题详情和答案>>
甲、乙、丙、丁为四种单质,其中两种为气体,且一种为黄绿色气体,A、B、C、D、E均为化合物,E常温下为无色液体,它们之间的转化关系如图所示:
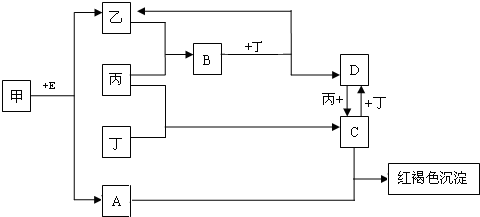
请回答下列问题
(1)写出下列物质的化学式:丁______,D______;
(2)检验C溶液中所含阳离子的试剂是:______,现象:______;
(3)丙与A溶液反应的离子方程式:______;
(4)C溶液与丁反应生成D的化学方程式:______.
查看习题详情和答案>>

请回答下列问题
(1)写出下列物质的化学式:丁______,D______;
(2)检验C溶液中所含阳离子的试剂是:______,现象:______;
(3)丙与A溶液反应的离子方程式:______;
(4)C溶液与丁反应生成D的化学方程式:______.
甲、乙、丙、丁为四种单质,其中两种为气体,且一种为黄绿色气体,A、B、C、D、E均为化合物,E常温下为无色液体,它们之间的转化关系如图所示:
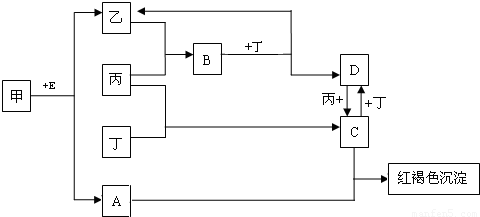
请回答下列问题
(1)写出下列物质的化学式:丁 ,D ;
(2)检验C溶液中所含阳离子的试剂是: ,现象: ;
(3)丙与A溶液反应的离子方程式: ;
(4)C溶液与丁反应生成D的化学方程式: . 查看习题详情和答案>>

请回答下列问题
(1)写出下列物质的化学式:丁 ,D ;
(2)检验C溶液中所含阳离子的试剂是: ,现象: ;
(3)丙与A溶液反应的离子方程式: ;
(4)C溶液与丁反应生成D的化学方程式: . 查看习题详情和答案>>
甲、乙、丙、丁为四种常见单质,常温下,乙、丙、丁为气体.丙常用于自来水消毒,甲是生活中常见金属,A在通常情况下为无色液体,B、C在溶液中反应.
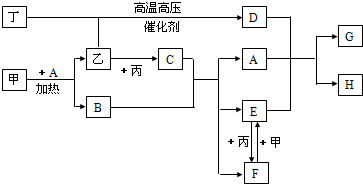
(1)D的化学式为
(2)甲+A反应的化学方程式为
(3)F+甲反应的离子方程式为
(4)A+D+E反应的离子方程式为
查看习题详情和答案>>

(1)D的化学式为
NH3
NH3
;闻气体丙的正确方法是扇闻
扇闻
;取少量长期放置的丙的水溶液,滴入几滴石蕊试液,可观察到的现象是溶液变红
溶液变红
.(2)甲+A反应的化学方程式为
3Fe+4H2O
Fe3O4+4H2
| ||
3Fe+4H2O
Fe3O4+4H2
.
| ||
(3)F+甲反应的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
;该反应中,证明甲适量或过量的方法是取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
取少量反应后的溶液于试管中,滴入几滴KSCN溶液,若溶液不变色,说明甲过量或适量
.(4)A+D+E反应的离子方程式为
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
Fe2++2NH3?H2O=Fe(OH)2↓+2NH4+
;该反应能顺利进行,是利用了D的极易溶于水且溶于水后显碱性
极易溶于水且溶于水后显碱性
的性质;若反应在试管中进行一,则其现象为先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
.