摘要:在20℃时氯化钠的溶解度为36.0g.现取一定量该温度下的饱和氯化钠溶液.用惰性电极电解.当阳极析出11.2L气体时.氯化钠完全消耗.所得溶液密度为1.20g/cm3.若忽略电极产生在溶液中的溶解.试计算: (1)电解时所取饱和氯化钠溶液的质量. (2)电解后溶液中氢氧化钠的物质的量浓度. 2007-2008学年度深圳宝安中学 新课标高一化学期末检测试卷 班级 姓名 学号 分数
网址:http://m.1010jiajiao.com/timu3_id_167352[举报]
在20 ℃时氯化钠的溶解度为36.0 g。现取一定量该温度下的饱和氯化钠溶液,用惰性电极电解。当阳极析出11.2 L (标准状况下)气体时,氯化钠完全消耗,所得溶液密度为1.20 g·cm-3。若忽略电极产物在溶液中的溶解,试计算:?
(1)电解时所取饱和氯化钠溶液的质量。
(2)电解后溶液中氢氧化钠的物质的量浓度。
查看习题详情和答案>>已知20℃时氯化钠的溶解度为36克.在该温度下,将碳酸钠与氯化钠的混合物17.2克,放入19克水中使其完全溶解,然后加入36.5克质量分数为20%的盐酸溶液,恰好完全反应.求:
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数.
查看习题详情和答案>>
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数.
已知20℃时氯化钠的溶解度为36克.在该温度下,将碳酸钠与氯化钠的混合物17.2克,放入19克水中使其完全溶解,然后加入36.5克质量分数为20%的盐酸溶液,恰好完全反应.求:
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数.
查看习题详情和答案>>
已知20℃时氯化钠的溶解度为36克.在该温度下,将碳酸钠与氯化钠的混合物17.2克,放入19克水中使其完全溶解,然后加入36.5克质量分数为20%的盐酸溶液,恰好完全反应.求:
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数.
查看习题详情和答案>>
(1)生成二氧化碳的质量
(2)反应后所得溶液的溶质的质量分数.
查看习题详情和答案>>
(2011?嘉兴模拟)氟化钠的用途非常广泛,可作杀菌剂、杀虫剂和木材防腐剂.实验室可通过下图所示的流程来制取:

请结合每小题的相关信息,回答下列有关问题:
(1)已知:饱和氟硅酸(H2SiF6)溶液为无色透明的发烟液体,密度为1.32g?mLˉ1,易挥发,有刺激性气味,与等物质的量浓度的H2SO4酸性相当,它对玻璃、陶瓷都有较强的腐蚀性.以上实验所用仪器全部用聚酯类材料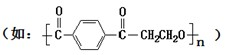 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
A.玻璃 B.铁 C.聚乳酸 D.陶瓷
(2)已知在20℃时Na2SiF6的溶解度为2.12g,请写出1L 1mol?Lˉ1的H2SiF6溶液与1L 1mol?Lˉ1Na2CO3溶液混合后(假设混合液中水的质量约等于2000g)发生化学反应的离子方程式为
(3)上述流程图中产生浑浊液的原因是生成了
A.NH4F B.H2SiO3 C.(NH4)2SiF6 D.(NH4)2CO3
(4)操作1后是否需要对沉淀进行洗涤
(5)溶液B中经操作
查看习题详情和答案>>

请结合每小题的相关信息,回答下列有关问题:
(1)已知:饱和氟硅酸(H2SiF6)溶液为无色透明的发烟液体,密度为1.32g?mLˉ1,易挥发,有刺激性气味,与等物质的量浓度的H2SO4酸性相当,它对玻璃、陶瓷都有较强的腐蚀性.以上实验所用仪器全部用聚酯类材料
 做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是
做成,在该类材料做成的容器中混合NH4HCO3固体、H2SiF6浓溶液和H2O时,加入试剂的顺序应是NH4HCO3固体、H2O和H2SiF6浓溶液
NH4HCO3固体、H2O和H2SiF6浓溶液
,加好试剂后,为了让它们充分反应,不能用C
C
棒搅拌(填字母).A.玻璃 B.铁 C.聚乳酸 D.陶瓷
(2)已知在20℃时Na2SiF6的溶解度为2.12g,请写出1L 1mol?Lˉ1的H2SiF6溶液与1L 1mol?Lˉ1Na2CO3溶液混合后(假设混合液中水的质量约等于2000g)发生化学反应的离子方程式为
2H++SiF62-+2Na++CO32-=Na2SiF6↓+CO2↑+H2O
2H++SiF62-+2Na++CO32-=Na2SiF6↓+CO2↑+H2O
.(3)上述流程图中产生浑浊液的原因是生成了
B
B
(填字母).A.NH4F B.H2SiO3 C.(NH4)2SiF6 D.(NH4)2CO3
(4)操作1后是否需要对沉淀进行洗涤
是
是
(填“是”或“否”),选择“是”或“否”的原因是使沉淀表面吸附的NH4F全部转移到溶液A中,提高产品产率
使沉淀表面吸附的NH4F全部转移到溶液A中,提高产品产率
.(5)溶液B中经操作
蒸发浓缩、冷却结晶、过滤
蒸发浓缩、冷却结晶、过滤
可得到副产品氯化铵;粗产品晶体经重结晶
重结晶
(填操作名称)可得纯净的产品.