摘要:26.现用30g普通冰醋酸(CH3COOH)与28g含有18O的乙醇(CH3CH218OH)在 浓硫酸存在的条件下加热制取乙酸乙酯.如果实际产量是理论产量的80%.可制取乙酸乙酯多少克?
网址:http://m.1010jiajiao.com/timu3_id_164886[举报]
 硝酸与金属反应时,浓度越稀还原产物价态越低.现用一定量的铝粉与镁粉组成的混合物与100ml硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示.回答下列问题:
硝酸与金属反应时,浓度越稀还原产物价态越低.现用一定量的铝粉与镁粉组成的混合物与100ml硝酸钾溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示.回答下列问题:(1)写出铝与混合溶液反应的离子方程式
8Al+30H++3NO3-=8Al3++3NH4++9H2O
8Al+30H++3NO3-=8Al3++3NH4++9H2O
(2)参加反应硝酸根离子物质的量为
0.006mol
0.006mol
mol(3)参加反应的铝与镁的质量之比为
3:4
3:4
(4)混合液中硫酸的物质的量的浓度为
0.36
0.36
mol/L.联氨(N2H4)及其衍生物是一类重要的火箭燃料,N2H4与N2O4反应能放出大量的热.
(1)已知:2NO2(g?N2O4(g);△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)?N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2的转化率的是
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00g N2H4与足量N2O4完全反应生成N2(g)和H2O,放出19.14kJ的热量.则反应:
2N2H4+N2O4═3N2(g)+4H2O的△H=-1224.96
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.030 0mol?L-1、c(N2O4)=0.012 0mol?L-1.计算反应2NO2(g?N2O4(g)的平衡常数K.
(4)现用一定量的Cu与足量的浓HNO3反应,制得上述1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
查看习题详情和答案>>
(1)已知:2NO2(g?N2O4(g);△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)?N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2的转化率的是
BC
BC
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00g N2H4与足量N2O4完全反应生成N2(g)和H2O,放出19.14kJ的热量.则反应:
2N2H4+N2O4═3N2(g)+4H2O的△H=-1224.96
-1224.96
-1224.96
kJ?mol-1.(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.030 0mol?L-1、c(N2O4)=0.012 0mol?L-1.计算反应2NO2(g?N2O4(g)的平衡常数K.
(4)现用一定量的Cu与足量的浓HNO3反应,制得上述1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
某课外活动小组为探究CO2与过量的NaOH溶液确实发生了化学反应,甲、乙、丙三位同学设计了下列三种实验装置,请回答下列问题:

(1)甲装置中CO2与过量的NaOH反应的离子方程式
(2)丙装置实验现象是
(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中安全性存在问题,该方案是
(4)请设计一个实验检验生成的产物Na2CO3中的阴离子.(简述操作步骤、所用试剂、实验现象和结论.)
(5)实验室中若需用44.8L(标准状态)CO2,现用含CaCO390%石灰石与足量的盐酸反应,至少需要这种石灰石
查看习题详情和答案>>

(1)甲装置中CO2与过量的NaOH反应的离子方程式
CO2+2OH-=CO32-+H2O
CO2+2OH-=CO32-+H2O
.(2)丙装置实验现象是
当NaOH溶液滴入锥形瓶之后,烧杯中的水倒吸入锥形瓶
当NaOH溶液滴入锥形瓶之后,烧杯中的水倒吸入锥形瓶
,解释产生该实验现象的原因NaOH与CO2反应,导致锥形瓶内压强降低,在大气压的作用下,烧杯中的水倒吸入锥形瓶
NaOH与CO2反应,导致锥形瓶内压强降低,在大气压的作用下,烧杯中的水倒吸入锥形瓶
.(3)甲、乙、丙同学设计的三个方案中,有一个方案在实际操作中安全性存在问题,该方案是
乙
乙
(填甲、乙或丙),原因是NaOH与CO2反应,锥形瓶内压强降低,在大气压的作用下,气球胀大,可能会发生爆炸
NaOH与CO2反应,锥形瓶内压强降低,在大气压的作用下,气球胀大,可能会发生爆炸
.(4)请设计一个实验检验生成的产物Na2CO3中的阴离子.(简述操作步骤、所用试剂、实验现象和结论.)
(5)实验室中若需用44.8L(标准状态)CO2,现用含CaCO390%石灰石与足量的盐酸反应,至少需要这种石灰石
222.2
222.2
g(结果保留一位小数).(2009?江苏)联氨(N2H4)及其衍生物是一类重要的火箭燃料.N2H4与N2O4反应能放出大量的热.
(1)已知:2NO2(g)═N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)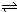 N2O4(g)达到平衡.
N2O4(g)达到平衡.
其他条件不变时,下列措施能提高NO2转化率的是
A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H=
(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol?L-1、c(N2O4)=0.0120mol?L-1.计算反应2NO2(g)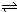 N2O4(g)的平衡常数K.
N2O4(g)的平衡常数K.
(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?
查看习题详情和答案>>
(1)已知:2NO2(g)═N2O4(g)△H=-57.20kJ?mol-1.一定温度下,在密闭容器中反应2NO2(g)
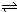 N2O4(g)达到平衡.
N2O4(g)达到平衡.其他条件不变时,下列措施能提高NO2转化率的是
BC
BC
(填字幕)A.减小NO2的浓度 B.降低温度 C.增加NO2的浓度 D.升高温度
(2)25℃时,1.00gN2H4(l)与足量N2O4(l)完全反应生成N2(g)和H2O(l),放出19.14kJ的热量.则反应2N2H4(l)+N2O4(l)=3N2(g)+4H2O(l)的△H=
-1224.96
-1224.96
kJ?mol-1(3)17℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.0300mol?L-1、c(N2O4)=0.0120mol?L-1.计算反应2NO2(g)
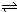 N2O4(g)的平衡常数K.
N2O4(g)的平衡常数K.(4)现用一定量的Cu与足量的浓HNO3反应,制得1.00L已达到平衡的N2O4和NO2的混合气体(17℃、1.01×105Pa),理论上至少需消耗Cu多少克?