摘要:22. (1)C10H16 6 4 2
网址:http://m.1010jiajiao.com/timu3_id_164507[举报]
金刚烷(C10H16)是一种重要的脂肪烷烃,其结构高度对称,如右图所示。金刚烷能与卤素发生取代反应,其中一氯 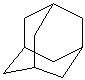 一溴金刚烷(C10H14ClBr)的同分异构体数目是
一溴金刚烷(C10H14ClBr)的同分异构体数目是
A.4种 B.6种 C.8种 D.10种
查看习题详情和答案>>下列各原子或离子的电子排布式错误的是( )
| A、K+ 1s22s22p63s23p6 | B、As 1s22s22p63s23p63d104s24p3 | C、N3- 1s22s22p6 | D、Cr 1s22s22p63s23p63d44s2 |
下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
①分离CCl4和H2O: ;
②除去澄清石灰水中悬浮的CaCO3: ;
③除去CaO固体中少量的CaCO3固体: ;
④从碘水中提取碘: ;
⑤分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物: .
查看习题详情和答案>>
A.分液 B.过滤 C.萃取 D.蒸馏 E.蒸发结晶 F.高温分解
①分离CCl4和H2O:
②除去澄清石灰水中悬浮的CaCO3:
③除去CaO固体中少量的CaCO3固体:
④从碘水中提取碘:
⑤分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:
某研究性学习小组对NaHCO3溶液进行如下探究.
Ⅰ探究NaHCO3溶液在不同温度下pH变化的原因
(1)小组同学测得饱和NaHCO3溶液在不同温度下的pH如下:
分析上述溶液pH增大的原因:
①甲同学认为是温度升高促进了HCO3-的水解,溶液pH增大.写出HCO3-水解的离子方程式: .
②乙同学认为溶液pH增大的原因还与NaHCO3在水溶液中受热分解产生Na2CO3有关.Na2CO3水解程度 (填“大于”或“小于”)NaHCO3.
③丙同学为验证甲、乙两同学的观点,进行了如下实验:
实验1:将加热后的溶液冷却至 10℃,测得此时溶液pH大于8.3;
实验2:在加热煮沸后已冷却的溶液中加入足量的试剂X,产生沉淀.
分析上述验证实验,可说明乙同学观点是 (填“合理”或“不合理”)的.
实验2中试剂X是 .
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
Ⅱ配制1.00mol?L-1NaHCO3溶液,测定其分解率
(2)配制1.00mol?L-1NaHCO3溶液100mL.容量瓶上可以看到的标记是 .
A.温度 B.容量 C.刻度线 D.溶液物质的量浓度
(3)小组同学取室温下已敞口放置一段时间的上述NaHCO3溶液50.00mL,与足量的稀盐酸反应,测定产生CO2的量,设计了如下装置.
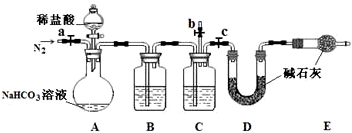
①上述装置C中盛装的试剂为 .
②往A中加入稀盐酸前,为赶出装置中的空气,先通入N2一段时间.此过程应进行的操作是 .
③若实验测得D装置增重 2.14g,则溶液中NaHCO3的分解率是 .
查看习题详情和答案>>
Ⅰ探究NaHCO3溶液在不同温度下pH变化的原因
(1)小组同学测得饱和NaHCO3溶液在不同温度下的pH如下:
| 温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却至 50℃ | pH | 8.3 | 8.4 | 8.5 | 8.8 |
①甲同学认为是温度升高促进了HCO3-的水解,溶液pH增大.写出HCO3-水解的离子方程式:
②乙同学认为溶液pH增大的原因还与NaHCO3在水溶液中受热分解产生Na2CO3有关.Na2CO3水解程度
③丙同学为验证甲、乙两同学的观点,进行了如下实验:
实验1:将加热后的溶液冷却至 10℃,测得此时溶液pH大于8.3;
实验2:在加热煮沸后已冷却的溶液中加入足量的试剂X,产生沉淀.
分析上述验证实验,可说明乙同学观点是
实验2中试剂X是
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清石灰水
Ⅱ配制1.00mol?L-1NaHCO3溶液,测定其分解率
(2)配制1.00mol?L-1NaHCO3溶液100mL.容量瓶上可以看到的标记是
A.温度 B.容量 C.刻度线 D.溶液物质的量浓度
(3)小组同学取室温下已敞口放置一段时间的上述NaHCO3溶液50.00mL,与足量的稀盐酸反应,测定产生CO2的量,设计了如下装置.

①上述装置C中盛装的试剂为
②往A中加入稀盐酸前,为赶出装置中的空气,先通入N2一段时间.此过程应进行的操作是
③若实验测得D装置增重 2.14g,则溶液中NaHCO3的分解率是
实验室需要0.10mol/L的硫酸920mL,某同学欲用密度为1.84g/cm3、溶质的质量分数为98%的浓硫酸进行配制.试回答:
(1)需选用
A.50mL B.100mL C.250mL D.1000mL
(2)需量取98%浓硫酸的体积为
(3)若提供如下仪器:
A.量筒 B.托盘天平 C.玻璃棒 D.容量瓶 E.胶头滴管 F.烧杯
完成该实验需选用哪些仪器?请按使用的先后顺序将仪器标号填在横线上:
(4)下列操作会使所配制的溶液物质的量浓度偏低的是
A.容量瓶洗净后未经干燥处理
B.向容量瓶转移溶液时,有少量液体溅出
C.加水时,水量超过了刻度线
(5)下列关于容量瓶的使用方法中,正确的是
A.使用前要检验是否漏水 B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中 D.向容量瓶中转移溶液要用玻璃棒引流.
查看习题详情和答案>>
(1)需选用
D
D
容量瓶(填序号).A.50mL B.100mL C.250mL D.1000mL
(2)需量取98%浓硫酸的体积为
5.4
5.4
mL.(3)若提供如下仪器:
A.量筒 B.托盘天平 C.玻璃棒 D.容量瓶 E.胶头滴管 F.烧杯
完成该实验需选用哪些仪器?请按使用的先后顺序将仪器标号填在横线上:
AFCDE
AFCDE
.(4)下列操作会使所配制的溶液物质的量浓度偏低的是
BC
BC
.A.容量瓶洗净后未经干燥处理
B.向容量瓶转移溶液时,有少量液体溅出
C.加水时,水量超过了刻度线
(5)下列关于容量瓶的使用方法中,正确的是
AD
AD
(填序号).A.使用前要检验是否漏水 B.在容量瓶中直接溶解固体或稀释液体
C.溶液未经冷却即注入容量瓶中 D.向容量瓶中转移溶液要用玻璃棒引流.