摘要:与0.96gSO2中氧原子个数相同的SO3为( )
网址:http://m.1010jiajiao.com/timu3_id_162852[举报]
下列各组比较项目包含的数据关系中,前者比后者大的是( )
| A、氯水与氨水中微粒种数 | B、H2O2与O2分子中氧氧键键能 | C、CH4分子与NH4+离子中的键角 | D、相同质量的铜片分别和过量浓硝酸、稀硝酸反应转移的电子数 |
已知A、B都是相对分子质量不超过250的有机物,A能发生如下反应:A+H2O→B+CH3COOH(已配平).B中C、H质量分数之和为50.1%,则B中氧原予数目最多为( )
| A、3 | B、4 | C、5 | D、6 |
(2009?宿迁模拟)工业合成氨与制备硝酸一般可连续生产,流程如图1:

在800℃、铂催化剂存在条件下,氨与氧气反应的主要产物是NO 和H2O.在实际生产中氨的氧化率与混合气中氧氨比(氧气与氨气物质的量比,以γ{n(O2)/n(NH3)}表示)的关系如图2所示.
请回答下列各题:
(1)若氨氧化率达到100%,理论上γ{n(O2)/n (NH3)}为1.25,而实际生产要将γ值维持在1.7~2.2之间,其原因是
(2)若使氨的氧化率达到95%,应控制氨在氨、空气混合气体中的体积分数约为
(设氧气占空气的体积分数为20%).将γ=1.75的氨、空气混合气体通入800℃、盛有铂催化剂的氧化炉,充分反应后导入到吸收塔的气体的主要成分是
(3)现以a mol NH3和足量空气为原料(不考虑N2的反应)最大程度制取NH4NO3,经过一系列转化反应后,向反应后的混合物中加入b g水,得到密度为ρ g?mL-1的溶液,计算该溶液中NH4NO3物质的量浓度可能的最大值
mol?L-1
mol?L-1.
查看习题详情和答案>>

在800℃、铂催化剂存在条件下,氨与氧气反应的主要产物是NO 和H2O.在实际生产中氨的氧化率与混合气中氧氨比(氧气与氨气物质的量比,以γ{n(O2)/n(NH3)}表示)的关系如图2所示.
请回答下列各题:
(1)若氨氧化率达到100%,理论上γ{n(O2)/n (NH3)}为1.25,而实际生产要将γ值维持在1.7~2.2之间,其原因是
一方面提高氧气量,增大氨的氧化率;另方面γ值在该范围,氨的氧化率已高达95~99%,再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本
一方面提高氧气量,增大氨的氧化率;另方面γ值在该范围,氨的氧化率已高达95~99%,再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本
.(2)若使氨的氧化率达到95%,应控制氨在氨、空气混合气体中的体积分数约为
10.5%
10.5%
(设氧气占空气的体积分数为20%).将γ=1.75的氨、空气混合气体通入800℃、盛有铂催化剂的氧化炉,充分反应后导入到吸收塔的气体的主要成分是
N2、NO2、H2O
N2、NO2、H2O
.(3)现以a mol NH3和足量空气为原料(不考虑N2的反应)最大程度制取NH4NO3,经过一系列转化反应后,向反应后的混合物中加入b g水,得到密度为ρ g?mL-1的溶液,计算该溶液中NH4NO3物质的量浓度可能的最大值
| 500aρ |
| 49a+b |
| 500aρ |
| 49a+b |
下列各组比较项目包含的数据关系中,前者比后者大的是( )
A.氯水与氨水中微粒种数
B.H2O2与O2分子中氧氧键键能
C.CH4分子与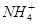 离子中的键角
离子中的键角
D.相同质量的铜片分别和过量浓硝酸、稀硝酸反应转移的电子数
查看习题详情和答案>>
(1)物质的量的符号为 ,科学实验表明:在0.012kg12C中所含的碳原子数约为 ,如果在一定量的粒子集体中所含的粒子数与0.012kg12C中所含的碳原子数相同,我们就说它为1摩尔,简称1摩,符号为 。
(2)现有下列10种物质:①Fe、 ②H2、 ③Fe2O3、④白酒、⑤酒精、⑥盐酸、⑦H2SO4、⑧NaCl、⑨NaHCO3、⑩H2O;
其中属于混合物的是 (填序号,下同),属于单质的是 ,属于氧化物的是 。
(3)当分散剂是水或其他液体时,如果按照分散质粒子的 来分,可以把分散系分为溶液、胶体和 ,区分溶液和胶体的常用方法是 。
(4)电解质是指在水溶液中或 下能够导电的 。电解质导电的根本原因在于它在这种状态下能够 出自由移动的离子。
查看习题详情和答案>>