摘要:17.HCl是 色气体.纯溴是红棕色的 体.碘在加热时会发生 . Na燃烧的火焰焰色是 色.Na2O2是 色的粉末.它与CO2反应放出的气体是 .具有漂白杀菌作用的物质是 .检验Cl-的方法是 .
网址:http://m.1010jiajiao.com/timu3_id_161990[举报]
实验室用下列仪器和药品制取纯净的无水CuCl2.
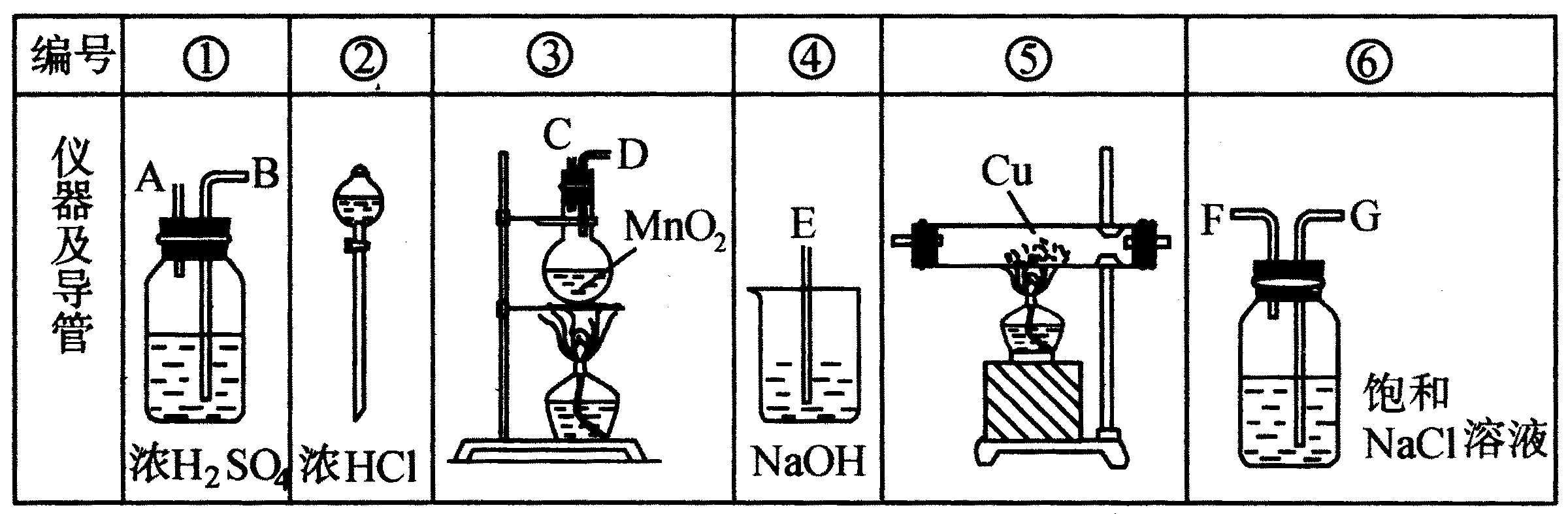
(1)如果所制气体为从左向右流向时,上述各仪器装置的正确连接顺序是(填写各装置的序号)( )接( )接( )接( )接( )接( );其中①与⑥装置相连时,玻璃接口应是________接________(用图中字母表示).
(2)实验开始时应首先检验装置的________;实验结束时应先熄灭________处酒精灯.
(3)装置①的作用是________;装置⑥的作用________;装置④中发生的反应的离子方程式为________.
(4)待充分反应后,装置⑤的玻璃管中剩余物呈________色.待冷却后,将所得产物配成溶液,溶液显________色.
(5)装置②选用分液漏斗盛装浓HCl,其作用是:________.
查看习题详情和答案>>某种混合气体可能有N2、HCl、CO,把混合气体依次通过足量的NaHCO3溶液和灼热的氧化铜粉未,气体体积都没有变化;再通过足量的过氧化钠固体,气体体积减小;最后经过铜网,经充分反应后气体体积又减少,但还有剩余气体.以下对混合气体组成的判断,正确的是( )
查看习题详情和答案>>
关于如图所示各装置的叙述中,不正确的是( )


| A、装置④可用于干燥、收集氨气,并吸收多余的氨气 | B、装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO、NO2等气体 | C、装置①中,d为阳极、c为阴极 | D、装置③中X若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸 |
有一白色固体混合物,可能含有的阴、阳离子分别是
为了鉴定其中的离子,现进行如下实验,根据实验现象,填写下列空格:
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12.由此可推出肯定不存在的离子是
(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出.由此可推出肯定存在的离子是
(3)尚待检验的离子是
查看习题详情和答案>>
| 阳离子 | K+ Ba2+ Ag+ Mg2+ NH4+ Na+ |
| 阴离子 | SO42- SO32- CO32- AlO2- |
(1)取该粉末,加水后得到无色溶液,且未嗅到气味;用pH试纸测得溶液的pH为12.由此可推出肯定不存在的离子是
NH4+、Ag+、Mg2+
NH4+、Ag+、Mg2+
.(2)向溶液中滴加盐酸溶液,开始有沉淀生成,继续滴加,沉淀消失,同时有无色无味气体逸出.由此可推出肯定存在的离子是
AlO2-、CO32-
AlO2-、CO32-
,肯定不存在的离子是Ba2+、SO32-
Ba2+、SO32-
.(3)尚待检验的离子是
Na+、K+、SO42-
Na+、K+、SO42-
,其检验方法通过焰色反应可以检验Na+、K+的存在,SO42-可以用盐酸酸化的BaCl2溶液检验
通过焰色反应可以检验Na+、K+的存在,SO42-可以用盐酸酸化的BaCl2溶液检验
.