网址:http://m.1010jiajiao.com/timu3_id_160964[举报]
| A.元素原子的最外层电予数等于元素的最高化合价 |
| B.电子层数相同的主族元素,最外层电子数多的原子半径小 |
| C.K、Mg、Al失电子能力和最高价氧化物水化物的碱性均依次增强 |
D.第三周期元素中,最外层电子数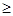 电子层数的为非金属元素 电子层数的为非金属元素 |
元素的原子结构决定其性质和周期表中的位置。下列说法正确的是
A.元素原子的最外层电予数等于 元素的最高化合价 元素的最高化合价 |
| B.电子层数相同的主族元素,最外层电子数多的原子半径小 |
| C.K、Mg、Al失电子能力和最高价氧化物水化物的碱性均依次增强 |
D.第三周期元素中,最外层电子数 电子层数的为非金属元素 电子层数的为非金属元素 |
|
元素的原子结构决定其性质和周期表中的位置.下列说法正确的是 | |
| [ ] | |
A. |
元素原子的最外层电予数等于元素的最高化合价 |
B. |
电子层数相同的主族元素,最外层电子数多的原子半径小 |
C. |
K、Mg、Al失电子能力和最高价氧化物水化物的碱性均依次增强 |
D. |
第三周期元素中,最外层电子数≥电子层数的为非金属元素 |
有原子序数依次增大的四种短周期元素A、B、C、D.已知:
①A元素有三种同位素A1、A2、A3.其中自然界里最多的一种同位素A1的质量数分别是A2的1/2、A3的1/3.
②常温下,B元素的气态氢化物的水溶液pH>7.
③C元素的质子数等于A元素与B元素两者的质子数之和.
④金属元素D的原子核内质子数比上一周期同主族元素多8个,且单质D不能从硫酸铜溶液中置换出铜.
请回答下列问题:
(1)C元素在周期表中的位置是________.
(2)比较B、C、D相应的简单离子的半径,由大到小的顺序为________.
(3)请写出单质D与硫酸铜溶液反应的化学方程式________.
(4)A、B两种元素可以形成多种化合物,其中有一种离子化合物A中两元素的原子个数比为1∶5,它的所有原子的最外层都符合相应稀有气体原子的最外层电子结构.写出A的电子式________.A物质与水反应生成一种碱和无色气体,写出有关的化学方程式________.
(一).对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法: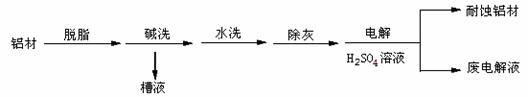
(1)碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出, 为将槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。 (填编号)
a.NH3 b.CO2 c.NaOH d.HNO3
(2)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,
阳极电极反应式为 。取少量废电解液,加入NaHCO3溶液,写出发生反应的离子方程式
(二).A—E五种元素中,除A、B外其他均为短周期元素它们的性质或原子结构如下表:
| 元素 | 元素性质或原子结构 |
| A | 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
| B | 单质为生活中常见的金属,其相对原子质量比A大8 |
| C | 地壳中含量最多的金属元素 |
| D | 元素的主族序数是其所在周期序数的3倍 |
| E | E的某种原子的原子核内没有中子 |
(1)在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a KJ热量,此反应的热化学方程式是
(2)A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
(3)向2mL 0.5mol/L的ACl3溶液中加入3mL 3mol/L KF溶液,
ACl3溶液褪成无色,再加入KI溶液和CCl4振荡后静置,CCl4层不显色,
则下列说法正确的是(已知氧化性Fe3+>I2) (填字母)。
a.A3+不与I-发生反应
b.A3+与F-结合生成不与I-反应的物质
c.F-使I-的氧化性减弱
d.A3+被F-还原为A2+,使溶液中不再存在A3+ 查看习题详情和答案>>