网址:http://m.1010jiajiao.com/timu3_id_160944[举报]
 (2013?泰安二模)处理主要包括水的净化、污水处理、硬水软化和海水淡化等.
(2013?泰安二模)处理主要包括水的净化、污水处理、硬水软化和海水淡化等.(1)水处理技术的核心是减少或除去水中的各种杂质离子.目前,
(2)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-,NO2-和CN-等有毒有害的还原性离子氧化除去.请写出ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式:
(3)地下水往往含有钙、镁的碳酸盐,自来水厂需要对地下水进行
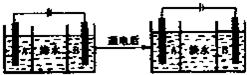
(4)海水的淡化是除去海水中所含的盐分,如图是海水利用电渗析法获得淡水的原理图,已知海水中含有Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.请回答:
①阳离子交换膜是指
②写出通电后阳极区的电极反应式

已知:(1)7.4g有机物A完全燃烧可产生0.4molCO2和0.5mol H2O,A蒸气对氢气的相对密度为37.核磁共振氢谱显示A中有5种类型氢原子的吸收峰,峰面积之比为3:3:2:1:1.
(2)
 (X代表卤原子)
(X代表卤原子)请回答下列问题:
(1)A的分子式是
(2)②的化学反应类型是
(3)①的化学反应方程式是
 +
+
| 浓硫酸 |
| △ |
 +H2O
+H2O +
+
| 浓硫酸 |
| △ |
 +H2O
+H2O(4)一定条件下,由G生成一种高分子树脂的化学方程式是
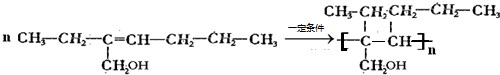
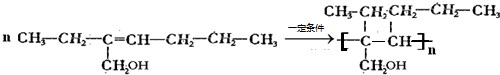
(5)检验有机物K中含有溴元素的实验操作是
(6)X有多种同分异构体,其中同时满足下列条件的同分异构体有


①苯环上有三个取代基,其中两个为相同基团;②1mol有机物可与2mol氢氧化钠水溶液完全反应得到两种有机产物.
(1)用电解方法制取钠时在
(2)工业上制取漂白粉的化学反应方程式为
(3)实验室有一瓶密封不严的漂白粉,其中肯定存在CaCl2,请设计实验,探究该固体中可能存在的其它物质.
①提出合理假设.
假设1:该漂白粉未变质,只含CaCl2和
假设2:该漂白粉全部变质,只含CaCl2和
假设3:该漂白粉部分变质,含有CaCl2、Ca(ClO)2和有CaCO3.
设计实验方案,进行实验.请在答题卡上写出实验步骤、预期现象与结论
限选用的仪器和药品:试管、滴管、带导管的单孔塞、蒸馏水、自来水、1mol/LHCl、品红溶液、新制澄清石灰水.
| 实验步骤 | 预期现象和结论 | ① | 取少量上述漂白粉于试管中, 加入足量1mol.L-1的HCl,并将产生的气体导入澄清石灰水中 加入足量1mol.L-1的HCl,并将产生的气体导入澄清石灰水中 . |
(1)若澄清石灰水 若澄清石灰水未变浑浊 若澄清石灰水未变浑浊 ,则样品中不含碳酸钙 样品中不含碳酸钙 ;(2)若澄清石灰水 若澄清石灰水 变浑浊 若澄清石灰水 变浑浊 ,则样品中含有碳酸钙 样品中含有碳酸钙 |
② | 向实验①后的试管中滴入 几滴品红溶液,振荡 几滴品红溶液,振荡 . |
若 若品红褪色,则样品中含Ca(ClO)2 若品红褪色,则样品中含Ca(ClO)2 ;若 若品红不褪色,则样品中不含Ca(ClO)2 若品红不褪色,则样品中不含Ca(ClO)2 ; |
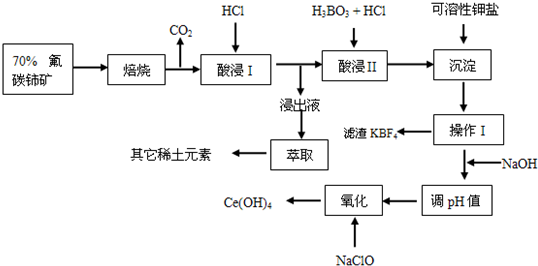
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;酸浸I的浸出液中含少量的+3价的铈
请回答下列问题
(1)焙烧前将矿石粉碎成细颗粒的目的是
(2)酸浸II后,四价铈转化为三价,为了避免三价铈以四氟硼酸盐形式损失,用可溶性钾盐将四氟硼酸根沉淀除去,该反应的离子方程式为:
(3)在生产过程中,酸浸I 中会产生大量黄绿色气体,污染环境、腐蚀设备,写出产生黄绿色气体的离子方程式:
(4)实验室中进行操作I所用玻璃仪器名称:
(5)写出氧化步骤的化学方程式:
(9分)NO分子因污染空气而臭名昭著。近年来,发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO亦被称为“明星分子”。
请回答下列问题。
(1)对NO的叙述正确的是________(填序号)。
A.NO是一种无色有毒的气体 B.常温、常压下,NO难与空气中的O2化合
C.含等质量氧元素的NO和CO的物质的量相等 D.NO易溶于水,不能用排水法收集
(2)NO对环境的危害在于________(填序号)。
A.破坏臭氧层 B.高温下能使一些金属被氧化 C.造成酸雨 D.与人体血红蛋白结合
(3)在含Cu+的酶的活化中心中,亚硝酸根离子可转化为NO。写出Cu+和亚硝酸根离子在酸性水溶液中反应的离子方程式为:_________________________________________。
(4)在常温下,把NO气体压缩到100个大气压,在一个体积固定的容器里加热到50℃,发现气体的压力迅速下降,压力降至略小于原压力的2/3就不再改变,已知其中一种产物为N2O,写出上述变化的化学方程式:___________________________________________。
(5)解释变化(4)中为什么最后的气体总压力小于原压力的2/3?
________________________________________________________________________
________________________________________________________________________。
查看习题详情和答案>>