摘要:16.(淡)黄绿色.Cl2,红.H+,褪色.HClO.
网址:http://m.1010jiajiao.com/timu3_id_160861[举报]
下列解释实验现象的反应方程式不正确的是( )
A.新制氯水中滴加NaOH溶液后,黄绿色褪去Cl2+2OH-=Cl-+ClO-+H2O
B.向NaHCO3 溶液中滴加酚酞溶液,溶液变红HCO3-?H++CO32-
C.向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+
D.向少量苯酚稀溶液中逐滴加入饱和溴水,生成白色沉淀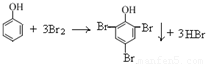
查看习题详情和答案>>
A.新制氯水中滴加NaOH溶液后,黄绿色褪去Cl2+2OH-=Cl-+ClO-+H2O
B.向NaHCO3 溶液中滴加酚酞溶液,溶液变红HCO3-?H++CO32-
C.向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+
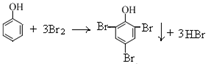
D.向少量苯酚稀溶液中逐滴加入饱和溴水,生成白色沉淀

查看习题详情和答案>>
下列解释实验现象的反应方程式不正确的是
- A.新制氯水中滴加NaOH溶液后,黄绿色褪去Cl2+2OH-=Cl-+ClO-+H2O
- B.向NaHCO3 溶液中滴加酚酞溶液,溶液变红HCO3-?H++CO32-
- C.向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀3Mg(OH)2+2Fe3+=2Fe(OH)3↓+3Mg2+
- D.向少量苯酚稀溶液中逐滴加入饱和溴水,生成白色沉淀
实验室用如图所示装置制备干燥纯净的氯气,并进行氯气的性质实验,请回答下列问题:
(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
(2)C中盛有饱和食盐水,其作用是
(3)E中盛有的Cl2 的颜色是
(4)F中是FeCl2 溶液,现象是
(5)G中是AgNO3溶液,现象是
(6)H中盛有NaOH溶液,其作用是
查看习题详情和答案>>

(1)A中盛有浓盐酸,B中盛有MnO2,则烧瓶中发生反应的化学方程式为:
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
| ||
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
.
| ||
(2)C中盛有饱和食盐水,其作用是
除去杂质氯化氢气体抑制C12在水中的溶解
除去杂质氯化氢气体抑制C12在水中的溶解
,D中浓硫酸的作用是除去水蒸气干燥Cl2
除去水蒸气干燥Cl2
.(3)E中盛有的Cl2 的颜色是
黄绿色
黄绿色
,Cl2 能使湿润的红色布条褪色的原因是因为氯气和水反应生成的次氯酸具有漂白性
因为氯气和水反应生成的次氯酸具有漂白性
.(4)F中是FeCl2 溶液,现象是
溶液从浅绿色变为棕黄色
溶液从浅绿色变为棕黄色
,发生反应的化学方程式为2FeCl2+Cl2=2FeCl3
2FeCl2+Cl2=2FeCl3
.(5)G中是AgNO3溶液,现象是
有白色沉淀生成
有白色沉淀生成
,有关化学反应的离子方程式为Cl-+Ag+=AgCl↓
Cl-+Ag+=AgCl↓
.(6)H中盛有NaOH溶液,其作用是
吸收多余的氯气
吸收多余的氯气
,发生反应的化学方程式为2NaOH+Cl2 =NaCl+NaClO+H2O
2NaOH+Cl2 =NaCl+NaClO+H2O
.