摘要:Ca(OH)2 过滤 Ca2++CO==CaCO3↓
网址:http://m.1010jiajiao.com/timu3_id_159989[举报]
在电解食盐水之前,需要提纯食盐水.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,正确的操作顺序是( )
①过滤
②加过量的NaOH溶液
③加适量的盐酸
④加过量的碳酸钠溶液
⑤加过量的氯化钡溶液.
①过滤
②加过量的NaOH溶液
③加适量的盐酸
④加过量的碳酸钠溶液
⑤加过量的氯化钡溶液.
查看习题详情和答案>>
为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作;①过滤 ②加过量的NaOH溶液 ③加适量盐酸 ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液.其中正确的操作顺序是
查看习题详情和答案>>
②⑤④①③或⑤②④①③
②⑤④①③或⑤②④①③
:为了除去粗盐中的Ca2+、Mg2+、S
及泥沙,可将粗盐溶于水,然后进行下列五项操作.其中正确的操作顺序是( )
①过滤
②加过量的NaOH溶液
③加适量盐酸
④加过量Na2CO3溶液
⑤加过量BaCl2溶液.
| O | 2- 4 |
①过滤
②加过量的NaOH溶液
③加适量盐酸
④加过量Na2CO3溶液
⑤加过量BaCl2溶液.
查看习题详情和答案>>
海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)以及通过氯碱工业获得烧碱和氯气等化工原料的生产流程简图: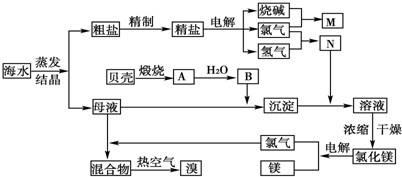
请回答:
(1)在粗盐中含有Ca2+、Mg2+、Fe3+、SO
等杂质,精制时所用的试剂为:a.盐酸 b.氯化钡溶液 c.氢氧化钠溶液 d.碳酸钠溶液.则加入试剂的顺序是(填编号) .
(2)氯碱工业为高耗能产业,一种用电解池燃料电池相结合的新工艺可节能30%.如图为工艺设计简图,根据图示回答以下问题:
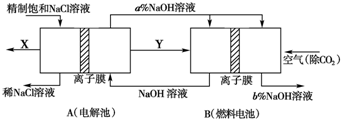
a.写出燃料电池中负极的电极反应式 .
b.比较NaOH溶液的浓度a b(填>、<、=)
(3)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,按所需的实验操作依次为 .
a.蒸馏 b.灼烧 c.过滤
d.在HCl气流中蒸发 e.冷却结晶
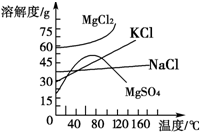
(4)母液中常含有MgCl2、NaCl、MgSO4、KCl等(其溶解度与温度的关系如图所示),可进一步加工制得一些重要的产品.若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是 ;过滤上述晶体后,将滤液降温到30℃以下,又逐渐析出晶体,用一定量的冷水洗涤该晶体,最后可得到比较纯净的 晶体.
(5)在母液中通入足量的Cl2,然后用热空气将Br2吹出,再用SO2吸收,写出此过程发生反应的化学反应方程式 .
查看习题详情和答案>>

请回答:
(1)在粗盐中含有Ca2+、Mg2+、Fe3+、SO
2- 4 |
(2)氯碱工业为高耗能产业,一种用电解池燃料电池相结合的新工艺可节能30%.如图为工艺设计简图,根据图示回答以下问题:

a.写出燃料电池中负极的电极反应式
b.比较NaOH溶液的浓度a
(3)Mg(OH)2中加入盐酸后,要获得MgCl2?6H2O晶体,按所需的实验操作依次为
a.蒸馏 b.灼烧 c.过滤
d.在HCl气流中蒸发 e.冷却结晶
(4)母液中常含有MgCl2、NaCl、MgSO4、KCl等(其溶解度与温度的关系如图所示),可进一步加工制得一些重要的产品.若将母液加热升温到60℃以上,随着水分的蒸发,会逐渐析出晶体,此晶体的主要成分是

(5)在母液中通入足量的Cl2,然后用热空气将Br2吹出,再用SO2吸收,写出此过程发生反应的化学反应方程式
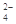 及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )
及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )