网址:http://m.1010jiajiao.com/timu3_id_157949[举报]
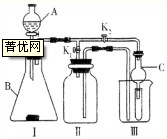
(1)利用装置Ⅰ、Ⅱ制取气体(K2关闭,K1打开).
甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,你认为是否正确
乙同学认为:利用装置Ⅱ作简易改进(不改变仪器装置),可收集NO2气体,改进的方法是
丙同学认为:利用装置Ⅱ作简易改进(改变仪器装置),可收集NO2气体,改进的方法是
(2)利用装置Ⅰ、Ⅲ验证物质的性质(K2打开,K1关闭).如设计实验证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,B中加
(14分)工业上利用CO和水蒸气在一定条件下发生反应制取氢气:
①CO(g)+H2O(g)  CO2(g)+H2(g) △H=-41 kJ/mol
CO2(g)+H2(g) △H=-41 kJ/mol
某小组研究在相同温度下该反应过程中的能量变化。他们分别在体积均为V L的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
| 容器编号 | 起始时各物质物质的量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||||
| CO | H2O | CO2 | H2 | ||||
| ① | 1 | 4 | 0 | 0 | t1 | 放出热量:32.8 kJ | |
| ② | 2 | 8 | 0 | 0 | t2 | 放出热量:Q | |
(2)容器①中反应达平衡时,CO的转化率为 %。
(3)计算容器②中反应的平衡常数K= 。
(4)下列叙述正确的是 (填字母序号)。
A.平衡时,两容器中H2的体积分数相等
B.容器②中反应达平衡状态时,Q > 65.6 kJ
C.反应开始时,两容器中反应的化学反应速率相等
D.容器①中,化学反应速率为:

(5)已知:②2H2 (g) + O2 (g) = 2H2O (g) ΔH=-484 kJ/mol,写出CO完全燃烧生成CO2的热化学方程式: 。
(6)容器①中反应进行到t min时,测得混合气体中CO2的物质的量为0.6 mol。若用200 mL 5 mol/L的NaOH溶液将其完全吸收,反应的离子方程式为(用一个离子方程式表示) 。
(7)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用图中所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。

①写出阳极所发生反应的电极反应式: 。
②在制备金属钛前后,CaO的总量不变,其原因是(请结合反应式解释) 。 查看习题详情和答案>>
某兴趣小组为探究氮的化合物的性质,设计了如图所示实验装置,A为气体发生装置。
按上图连接好各仪器,检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的无色气体通过后面装置。片刻后可观察到F中铜片慢慢溶解。请回答下列问题:
(1)A制备气A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2)相对应的装置可以是________(填字母)。
(2)写出题干装置C中发生反应的化学方程式________,C处加热片刻后撤去酒精灯,铂丝仍保持红热,原因是________________________________________。
(3)铜片完全溶解后,发现F装置中溶液呈绿色,加水稀释后呈蓝色,有同学得出两种结论:①浓Cu(NO3)2溶液呈绿色,稀Cu(NO3)2溶液呈蓝色;②Cu(NO3)2溶液呈蓝色,呈绿色是由于溶液溶解过量的NO2,试设计实验验证哪一种结论正确______________________________________________________________。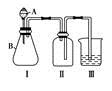 (4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题:
(4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题:
①甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,理由是______________________________________________。
②乙同学认为:利用装置Ⅱ作简易改进(不改变仪器装置),可收集NO、O2,改进的方法是__________________________________________。

按上图连接好各仪器,检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的无色气体通过后面装置。片刻后可观察到F中铜片慢慢溶解。请回答下列问题:
(1)A制备气A中所用试剂,从下列固体物质中选取:①NH4HCO3、②NH4Cl、③Ca(OH)2)相对应的装置可以是________(填字母)。
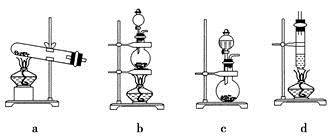
(2)写出题干装置C中发生反应的化学方程式________,C处加热片刻后撤去酒精灯,铂丝仍保持红热,原因是________________________________________。
(3)铜片完全溶解后,发现F装置中溶液呈绿色,加水稀释后呈蓝色,有同学得出两种结论:①浓Cu(NO3)2溶液呈绿色,稀Cu(NO3)2溶液呈蓝色;②Cu(NO3)2溶液呈蓝色,呈绿色是由于溶液溶解过量的NO2,试设计实验验证哪一种结论正确______________________________________________________________。
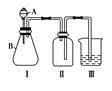 (4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题:
(4)该兴趣小组同学共同设计了如图所示的实验装置,利用装置Ⅰ、Ⅱ制取气体,请回答下列问题:①甲同学认为:利用装置Ⅱ可以收集H2、NH3等气体,但不能收集O2和NO,理由是______________________________________________。
②乙同学认为:利用装置Ⅱ作简易改进(不改变仪器装置),可收集NO、O2,改进的方法是__________________________________________。
| 流程1:气化炉中产生H2 | 流程2:燃烧炉中CaO再生 |
| 通入水蒸气,主要化学反应: ①C(s)+H2O(g)=CO(g)+H2(g) △H=+131.6kJ?mol-1 ②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.2kJ?mol-1 ③CaO(s)+CO2(g)=CaCO3(s) △H=-178.3kJ?mol-1 |
通入纯氧,主要化学反应: ④C(s)+O2(g)=CO2(g) △H=-393.8kJ?mol-1 ⑤CaCO3(s)=CaO(s)+CO2(g) K |
(1)气化炉中总反应:C(s)+2H2O(g)+CaO(s)=CaCO3(s)+2H2(g)△H=
(2)燃烧炉中反应⑤所需的能量由反应④提供.如果再生1mol CaO,至少需通入纯氧
(3)当只改变温度或压力时,反应⑤有如图所示的变化:
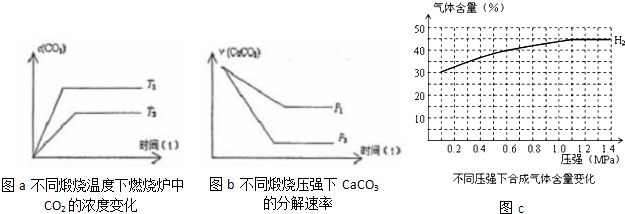
图a推知T1
图b推知P1
(4)在一定温度、不同压力时,气化炉中H2的变化量约等于CO的变化量(即△n(H2)=△n(CO)),当起始c(H2):c(CO)=3:2时,请根据n(H2)变化,补充完整图C中n(CO)图示变化.
(5)一定条件下,气化炉中的各反应达到平衡状态,采取以下措施可以提高H2产量的是
A.反应②中使用合适的催化剂 B.不断移走CaCO3,并升高气化炉内的温度
C.适当增加水蒸气的通入量 D.增加CaO的量,提高CO2的吸收率
(6)写出一条这种制H2技术的优点