摘要:7.有一FeSO4.Fe2(SO4)3的混合物.经测定其中含硫质量分数为22.73%.则此混合物中 FeSO4与Fe2(SO4)3物质的量之比为 ( ) A.1:1 B.1:2 C.2:1 D.2:2
网址:http://m.1010jiajiao.com/timu3_id_157689[举报]
有一FeSO4、Fe2(SO4)3的混合物,经测定其中含硫质量分数为22.73%,则此混合物中FeSO4与Fe2(SO4)3的物质的量之比为
- A.1∶1
- B.1∶2
- C.2∶1
- D.2∶3
有一FeSO4、Fe2(SO4)3的混合物,经测定其中含硫质量分数为22.73%,则此混合物中FeSO4与Fe2(SO4)3的物质的量之比为( )
A.1∶1 B.1∶2
C.2∶1 D.2∶3
查看习题详情和答案>>
(2010?宝鸡三模)三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某化学实验小组对组成可能为Fe2O3、Cu2O或二者混合物的红色粉末进行了一系列的实验.
请回答实验中有关问题:
实验一:探究红色粉末的成分
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO.
②Cu能与Fe2(SO4)3溶液作用生成CuSO4和FeSO4.
[提出假设]假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN溶液.
(1)若假设1成立,则实验现象是
(2)若假设2成立,则实验现象是
(3)若固体粉末完全溶解,滴加KSCN溶液时溶液不变红色,则此时发生反应的离子方程式为
[实验结果]经实验分析,假设3是正确的.
实验二:测定Cu2O的质量分数
(4)取a g该固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为
×100%
×100%.
实验三:利用该红色粉末制取较纯净的胆矾(CuSO3?5H2O)
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下表:
实验室可供选择试剂有:A.氨水 B.H2O2 C.NaOH D.Cu2(OH)2CO3
该实验小组设计实验方案如下:
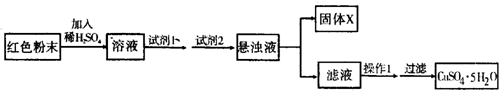
(5)请回答:
①试剂1为
②试剂2为
③固体X的化学式为
④操作I为
查看习题详情和答案>>
请回答实验中有关问题:
实验一:探究红色粉末的成分
[查阅资料]①Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4,在空气中加热生成CuO.
②Cu能与Fe2(SO4)3溶液作用生成CuSO4和FeSO4.
[提出假设]假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3和Cu2O的混合物
[设计探究实验]取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN溶液.
(1)若假设1成立,则实验现象是
固体完全溶解,溶液呈血红色
固体完全溶解,溶液呈血红色
.(2)若假设2成立,则实验现象是
溶液变为蓝色,最终溶液中仍有红色固体
溶液变为蓝色,最终溶液中仍有红色固体
.(3)若固体粉末完全溶解,滴加KSCN溶液时溶液不变红色,则此时发生反应的离子方程式为
Fe2O3+6H+═2Fe3++3H2O、Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+
Fe2O3+6H+═2Fe3++3H2O、Cu2O+2H+═Cu+Cu2++H2O、2Fe3++Cu═2Fe2++Cu2+
.[实验结果]经实验分析,假设3是正确的.
实验二:测定Cu2O的质量分数
(4)取a g该固体粉末在空气中充分加热,待质量不再变化时,称其质量为b g(b>a),则混合物中Cu2O的质量分数为
| 9(b-a) |
| a |
| 9(b-a) |
| a |
实验三:利用该红色粉末制取较纯净的胆矾(CuSO3?5H2O)
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下表:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
该实验小组设计实验方案如下:

(5)请回答:
①试剂1为
B
B
(从可供选择试剂中选择并填出对应字母编号,②同);②试剂2为
D
D
;③固体X的化学式为
Fe(OH)3
Fe(OH)3
;④操作I为
加热浓缩,冷却结晶
加热浓缩,冷却结晶
.细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”。其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O 2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O 15FeSO4+ 8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2 2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: 。
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3] | | |
| 步骤4 | 洗涤 | |
| 步骤5 | | 得到FeSO4溶液 |
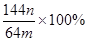 。该学生的计算是否正确: ,请说明理由 。
查看习题详情和答案>>
。该学生的计算是否正确: ,请说明理由 。
查看习题详情和答案>>
细菌冶金是一种新工艺,其能耗少、减少环境污染.称为“绿色冶金”。其原理:①氧化硫硫杆菌和聚硫杆菌能把矿石中的硫氧化成硫酸,反应式为2S+3O2+2H2O 2H2SO4,②氧化亚铁硫杆菌在上面产生的硫酸中能把硫酸亚铁氧化成硫酸铁③细菌得到了所需要的能量,生成的硫酸铁可把FeS2(黄铁矿)和Cu2S(辉铜矿)等转变为可溶性化合物而从矿石中溶解出来,其化学过程是:
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O 15FeSO4+ 8H2SO4
Cu2S(辉铜矿)+2Fe2(SO4)2 2CuSO4+4FeSO4+S
(1)写出②反应的化学方程式: 。
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
实验室有下列试剂可供选择A.H2O2 B.CaO C.CuO D.稀H2SO4 E.铁粉;
实验经过滤后还需设计的实验操作步骤和目的是:
(3)若向CuSO4、FeSO4混合液中加入适量碱液,将溶液蒸干、灼烧得到红色粉末是Fe2O3、Cu2O混合物,欲测定该混合物中Cu2O的质量分数。该实验小组的方法是向m g混合物中加人足量的稀硫酸,经过滤、洗涤、干燥、称量固体的质量为n g。已知Cu2O溶于稀硫酸生成Cu和CuSO4。某学生据此计算出该混合物Cu2O的质量分数的计算式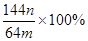 。该学生的计算是否正确: ,请说明理由 。
。该学生的计算是否正确: ,请说明理由 。
Fe2S2(黄铁矿)+7Fe2(SO4)3+8H2O
Cu2S(辉铜矿)+2Fe2(SO4)2
(1)写出②反应的化学方程式: 。
(2)某实验小组,欲将硫酸铜和硫酸亚铁的酸性混合液分离出硫酸亚铁溶液.经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如表2
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验经过滤后还需设计的实验操作步骤和目的是:
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3] | | |
| 步骤4 | 洗涤 | |
| 步骤5 | | 得到FeSO4溶液 |
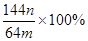 。该学生的计算是否正确: ,请说明理由 。
。该学生的计算是否正确: ,请说明理由 。