网址:http://m.1010jiajiao.com/timu3_id_157357[举报]
Ⅰ 粗食盐常含有少量K+、Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下

① 欲除去溶液Ⅰ中的Ca2+、Mg2+、SO42-离子,选出a所代表的试剂,按滴加顺序依次为
____________(只填化学式)。
②洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为__________________。
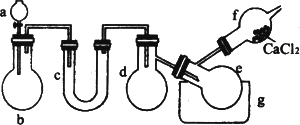
③在整个实验过程中,下列实验装置不可能用到的是_____________(填序号)。


Ⅱ 我国化学工程专家侯德榜创立的侯氏制碱法,食盐是其中的主要原料。实验室根据侯氏制碱法并参考下表数据,制备纯碱的主要步骤是:将配置好的NaCl饱和溶液倒入烧杯中加热,控制一定温度范围,搅拌下分批加入研细的NH4HCO3固体,加料完毕后,继续保温30min,静置、过滤得晶体NaHCO3。用少量蒸馏水洗涤除去杂质,抽干后,转入蒸发皿中,灼烧2h,制得Na2CO3固体。

操作过程中反应温度控制在30℃ <t<_______为控制此温度范围,采取的加热方式为________________。
Ⅲ 电解饱和食盐水的装置如图所示,若收集的H2为2L,则同样条件下收集的Cl2 ________ (填“>”、“=”或 “<”)2L,原因是___________________ 。装置改进后,可用于制备NaOH溶液,若测定溶液中 NaOH的浓度,常用的方法为________________。装置b口出来气体的检验方法:_______________________。

在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是( )
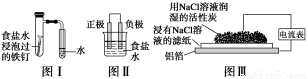
A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管
B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁
C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑
D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑
查看习题详情和答案>>
| |||||||||||||||||||||||||||||||||||||||||||||||
在日常生活中,我们经常看到铁制品生锈、铝制品表面出现白斑等众多的金属腐蚀现象。可以通过下列装置所示实验进行探究。下列说法正确的是( )
| A.按图Ⅰ装置实验,为了更快更清晰地观察到液柱上升,可采用下列方法:用酒精灯加热具支试管 |
| B.图Ⅱ是图Ⅰ所示装置的原理示意图,图Ⅱ的正极材料是铁 |
| C.铝制品表面出现白斑可以通过图Ⅲ装置进行探究,Cl-由活性炭区向铝箔表面区迁移,并发生电极反应:2Cl--2e-=Cl2↑ |
| D.图Ⅲ装置的总反应为4Al+3O2+6H2O=4Al(OH)3,生成的Al(OH)3进一步脱水形成白斑 |
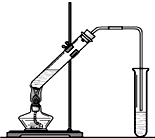 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯.回答下列问题:(1)乙醇、乙酸分子中的官能团分别是
(2)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
(3)该反应属于哪类反应类型
A.加成反应 B.取代反应 C.水解反应
D.酯化反应 E.可逆反应
(4)写出制取乙酸乙酯的化学反应方程式
(5)无水乙酸又称冰醋酸(熔点16.6℃).在室温较低时,无水乙酸就会凝结成像冰一样的晶体.请简单说明在实验中若遇到这种情况时,你将如何从试剂瓶中取出无水乙酸?
(6)乙醇在一定条件下还能发生脱水反应产生乙烯.乙烯通入溴的四氯化碳溶液中,观察到的现象是
此外,乙烯能用来生产环氧乙烷,生产工艺主要有两种:
工艺一:CH2=CH2+Cl2+O2→
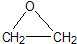 +CaCl2+H2O
+CaCl2+H2O工艺二:2CH2=CH2+O2
| Ag |
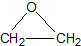
根据绿色化学的原则,理想的生产工艺是原子经济性好的反应,因此,在实际生产中,应采用