网址:http://m.1010jiajiao.com/timu3_id_155447[举报]
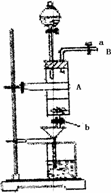
(13分)如右图所示,中学化学实验室采用该装置用于制备乙酸乙酯。
⑴写出制备乙酸乙酯的化学方程式 ▲ 。
 ⑵浓硫酸在实验中的作用是 ▲ 、 ▲ 。
⑵浓硫酸在实验中的作用是 ▲ 、 ▲ 。
⑶加热一段时间后,在试管B饱和碳酸钠溶液的液面上方有一 层油层,在油、水交界处观察到有气泡产生,气泡的主要成分是 ▲ 。
⑷停止加热,取下试管B ,嗅闻管内液体气味,闻到更多的是刺激性气味,这是因为物质的挥发等因素导致产品混有杂质,如 ▲ 和 ▲ 等,为进一步验证产物中某些杂质存在,在保持试管B相对稳定情况下,沿试管内壁滴入紫色石蕊试液,静置片刻会在试管内油层下方明显看到液体呈现三种颜色,由上而下分别为红色、紫色、蓝色,其原因可能是 ▲ ,故产品需进行提纯。
⑸已知乙醇能和氯化钙结合。将所得产品依次用饱和碳酸钠溶液、饱和食盐水、饱和氯化钙溶液洗涤油层,分别分液。用饱和食盐水洗涤去除油层中可能含有的 ▲ 杂质,减少乙酸乙酯的溶解,并防止对下面操作产生不利影响。
⑹在上述操作后,在所得油状液体中加入无水硫酸钠充分振荡,倾倒出油状液体,再进行 ▲ (填提纯的操作方法),收集74~78℃的馏分即可获得较纯净的乙酸乙酯。
查看习题详情和答案>>
| |||||||||||||||||||||||
化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验
(一)设计如下图所示装置I制备和收集干燥纯净的氯气以备后续实验:
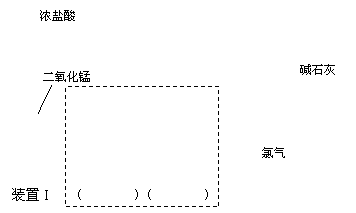

①烧瓶中发生反应的离子方程式为: ;
②请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;

 (二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
(二)在右图所示装置II中,在试管中先加入过量铁粉,再滴入少量CuSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
①检查制取氢气装置气密性的操作方法是
②当点燃氢气后,将导管伸入盛有氯气的集气瓶中,观察到的现象是
③试管中加入少量CuSO4溶液的作用是 ,其原理是
(三)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验,A组同学发现制取氢气后的试管中还有较多固体剩余。同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生。请解释可能原因(用离子方程式表示):
;B组同学向集气瓶中注入适量水,用力振荡后,向其中滴入少量Na2S2O3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。(已知Na2S2O3+ H2SO4= Na2SO4+S↓+SO2↑+ H2O),同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①
②
查看习题详情和答案>>(9分)某化学兴趣小组在实验室制取漂白粉,并探究氯气与石灰乳反应的条件和产物。

该兴趣小组设计了上述实验装置进行实验
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2。
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:
 3Cl2+6OH-
3Cl2+6OH-![]() 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O
请回答下列问题:
(1)①乙装置的作用是
②写出丁装置中发生反应的化学方程式
③该兴趣小组用100mL 12mol/L盐酸与8.7g MnO2制备氯气,并将所得氯气与过量的石灰乳反应,则理论上最多可制得Ca(ClO)2______________g。
(2)小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,部分氯气未与石灰乳反应而逸出,以及温度升高是可能原因。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示为右图(不考虑氯气和水的反应)。
①图中曲线I表示_____________离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为______________mol。
(3)为了提高Ca(ClO)2的产率,可对丙装置作适当改进。请你给出一种改进方法 。
查看习题详情和答案>>(14分) 实验室需要少量某些气体时,通常使用快速的方法制备。下列几个实验可快速制取实验事所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
实验室需要少量某些气体时,通常使用快速的方法制备。下列几个实验可快速制取实验事所需的少量气体,并进行相关性质实验。(实验装置如右图所示)
(1)若A中为15的H2O2溶液,B中固体为MnO2,C中盛有FeCl2和KSCN的混合液。回答下列问题:
① 装置A的名称是_________。
② 旋开E后,C中的现象是 ________。
③ 假设15的H2O2溶液和30的H2O2溶液的密度均为1g/cm3;如何用30H2O2溶液配制100克15的H2O2溶液:_______ 。
(2)若B中是生石灰,将A中液体逐滴加入B内,实验中观察到C的溶液中先出现沉淀、然后沉淀逐渐溶解,当溶液恰好澄清时,关闭E,将C装置放入盛有沸水的烧杯中,静置片刻,观察到试管内壁出现光亮的银镜。回答下列问题:
① C中是葡萄糖与__________(写化学式)的混合液。
② 仪器D在此实验中的作用是___________________。
(3)若A中浓盐酸,B中装有固体KMnO4,C中盛有KI淀粉溶液,旋开E后,B中出现黄绿色气体,C中的现象是先出现蓝色后褪色.
甲同学认为:Cl2溶于水生成HClO, HClO具有漂白性。
乙同学认为:氯水具有强氧化性,把I2氧化IO3-。
丙同学为了证明甲、乙同学的观点谁的正确,做了如下实验:取C中褪色的溶液少许,加几滴淀粉溶液,结果溶液不变蓝色。则_________(填甲、乙同学)的观点正确。
有学生认为,此实验装置存在不足,请你指出________________________________ 查看习题详情和答案>>