网址:http://m.1010jiajiao.com/timu3_id_155396[举报]
摄影胶卷上涂布的感光材料主要是AgBr。在照相时按动快门一瞬间,进入相机的光使AgBr发生了分解反应2AgBr![]() 2Ag+Br2。由于进光量极少,分解出的Ag极少,所以必须通过化学方法进行显影才能看到底片上的影像。对苯二酚是一种常用的显影剂,在显影时发生了如下变化:
2Ag+Br2。由于进光量极少,分解出的Ag极少,所以必须通过化学方法进行显影才能看到底片上的影像。对苯二酚是一种常用的显影剂,在显影时发生了如下变化:

(1)曝光时所产生的微量Ag在显影过程中_________。
(A)是氧化剂 (B)是还原剂
(C)起催化剂的作用 (D)不起什么作用
(2)显影液中如果只溶有对苯二酚,显影速度则非常缓慢。为提高显影速度,可加入_________。
(A)Na2SO4 (B)Na2SO3 (C)Na2CO3 (D)Na2S2O3
(3)溶于显影液中的氧气能与对苯二酚反应,最终生成棕褐色的污斑,影响底片的质量。
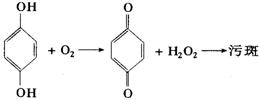
为避免形成污斑,可向显影液中加入_________。
(A)Na2SO4 (B)Na2SO3 (C)Na2CO3 (D)Na2S2O3
查看习题详情和答案>>A.2H2O![]() 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2![]() 2H2O
2H2O
B.NH3+CO2+H2O====NH4HCO3,NH4HCO3![]() NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑
C.H2+I2![]() 2HI,2HI
2HI,2HI![]() H2↑+I2↑
H2↑+I2↑
D.2Ag+Br2![]() 2AgBr,2AgBr
2AgBr,2AgBr![]() 2Ag+Br2
2Ag+Br2
下列各组反应中,属于可逆反应的一组是( )
A.2H2O![]() 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2![]() 2H2O
2H2O
B.NH3+CO2+H2O====NH4HCO3,NH4HCO3![]() NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑
C.H2+I2![]() 2HI,2HI
2HI,2HI![]() H2↑+I2↑
H2↑+I2↑
D.2Ag+Br2![]() CuO2AgBr,2AgBr
CuO2AgBr,2AgBr![]() 2Ag+Br2
2Ag+Br2
|
下列各组反应中,属于可逆反应的一组是 | |
A. |
2H2O |
B. |
NH3+CO2+H2O |
C. |
H2+I2 |
D. |
2Ag+Br2 |