摘要: Na+ H2O
网址:http://m.1010jiajiao.com/timu3_id_154173[举报]
(1)在反应MnO2 + 4HCl = MnCl2 + 2H2O +Cl2↑中,
①用双线桥法标出电子转移的方向和数目:__________________________
②还原剂是_______________;
③HCl中,被氧化的Cl原子与未被氧化的Cl原子个数比是__________________。
④若要产生112 mL氯气,则转移的电子数目是____________________。
(2) 已知金属钠投入水中能发生下列反应2Na+2H2O==2NaOH+H2↑。现将2.3g钠投入水中,充分反应后。则n(NaOH )=___________;V(H2)=_____________(标准状况下);假设反应后得到的溶液中Na+与水分子的个数比为1:100,则反应所需的m(H2O)=________
查看习题详情和答案>>
①用双线桥法标出电子转移的方向和数目:__________________________
②还原剂是_______________;
③HCl中,被氧化的Cl原子与未被氧化的Cl原子个数比是__________________。
④若要产生112 mL氯气,则转移的电子数目是____________________。
(2) 已知金属钠投入水中能发生下列反应2Na+2H2O==2NaOH+H2↑。现将2.3g钠投入水中,充分反应后。则n(NaOH )=___________;V(H2)=_____________(标准状况下);假设反应后得到的溶液中Na+与水分子的个数比为1:100,则反应所需的m(H2O)=________
海水资源的利用具有广阔前景.海水中主要离子的含量如下:
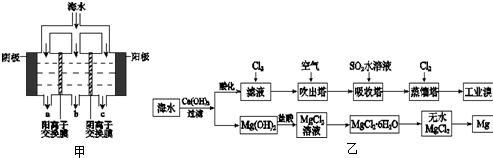
(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是
②在阴极附近产生少量白色沉淀,其成分有
③淡水的出口为
(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是
②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是
③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
查看习题详情和答案>>
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42 | 2560 | Br- | 64 |
| Mg2+ | 1272 |

(1)电渗析法淡化海水示意图如图甲所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过.
①阳极主要电极反应式是
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
.②在阴极附近产生少量白色沉淀,其成分有
Mg(OH)2
Mg(OH)2
和CaCO3,生成CaCO3的离子方程式是Ca2++OH-+HCO3-=CaCO3↓+H2O
Ca2++OH-+HCO3-=CaCO3↓+H2O
.③淡水的出口为
b
b
(填“a”、“b”或“c”).(2)利用海水可以提取溴和镁,提取过程如图乙所示:
①提取溴的过程中,经过2次Br-→Br2转化的目的是
对溴元素进行富集
对溴元素进行富集
,吸收塔中发生反应的离子方程式是SO2+Br2+2H2O=4H++2Br-+SO42-
SO2+Br2+2H2O=4H++2Br-+SO42-
.解释通空气的目的是通入空气将Br2蒸气带出,使Br2(g)?Br2(aq)或Br2+H2O?HBr+HBrO平衡向左移动
通入空气将Br2蒸气带出,使Br2(g)?Br2(aq)或Br2+H2O?HBr+HBrO平衡向左移动
.②从MgCl2溶液中得到MgCl2?6H2O晶体的主要操作是
加热浓缩、冷却结晶
加热浓缩、冷却结晶
、过滤、洗涤、干燥.③依据上述流程,若将10m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为
179.2
179.2
L(忽略Cl2溶解).