摘要:已知某酸性溶液中含有Ba2+.Mg2+.则下述离子组中能与上述离子共存的是 A.CO32-.Cl- B.NO3-.Cl- C.NO3-.SO42- D.OH-.NO3-
网址:http://m.1010jiajiao.com/timu3_id_153547[举报]
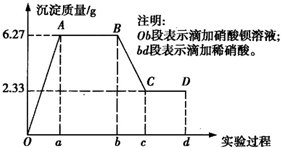 某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO
某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO2- 3 |
2- 4 |
(1)水样中一定含有的阴离子是
SO42-,CO32-
SO42-,CO32-
,其物质的量浓度之比为1:2
1:2
.(2)写出BC段所表示反应的离子方程式:
BaCO3+2H+=Ba2++CO2↑+H2O
BaCO3+2H+=Ba2++CO2↑+H2O
.(3)由B到C点变化过程中消耗硝酸的体积为
40ml
40ml
.(4)试根据实验结果推测K+是否存在?
是
是
(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是≥0.6mol/L
≥0.6mol/L
.(若K+不存在,则不必回答该问).(5)设计简单实验验证原水样中可能存在的离子:
取少量水样与试管中,向试管中加入过量升温硝酸钡溶液和稀硝酸,待沉淀完全和无气体生成后,向上层清液中滴加适量的硝酸银溶液,若生成白色沉淀,则原水样中 含有Cl-,若无白色沉淀生成,证明无Cl-存在
取少量水样与试管中,向试管中加入过量升温硝酸钡溶液和稀硝酸,待沉淀完全和无气体生成后,向上层清液中滴加适量的硝酸银溶液,若生成白色沉淀,则原水样中 含有Cl-,若无白色沉淀生成,证明无Cl-存在
.(写出实验步骤、现象和结论)(1)一瓶澄清的溶液,其中可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO42-、CO32-、NO3-、I-,取该溶液进行以下实验:
a.用pH试纸测得该溶液呈酸性;
b.取部分溶液,加入数滴新制的氯水及少量CCl4,经振荡、静置后,CCl4层呈紫红色;
c.另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐变为碱性,在整个滴加过程中无沉淀生成;
d.取部分上述碱性溶液,加入Na2CO3溶液,有白色沉淀生成,
e.将c得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定:
①写出b所发生反应的离子方程式 ;
②该溶液中肯定存在的离子是 ;
③该溶液中肯定不存在的离子是 。
(2)某反应体系中反应物与生成物有: K2SO4、CaSO4、MnSO4、CaC2O4、KMnO4、H2SO4、H2O和一种未知气体X。
①已知CaC2O4在反应中失去电子,则该反应的氧化剂是 。
②在标准状况下生成11.2LX时,有0.5mol 电子转移,共消耗0.25mol CaC2O4,X的化学式为 。
查看习题详情和答案>>