网址:http://m.1010jiajiao.com/timu3_id_148103[举报]
下列变化前后的数据关系不符合a > b的是( )
A.一瓶浓硫酸溶质的质量分数为a,敞口放置一段时间后溶质质量分数为b
B.一瓶浓盐酸的质量为a,敞口放置一段时间后质量为b
C.将锌片放置在质量为a的硫酸铜溶液中,一段时间后,溶液质量为b
D.酒精和水混合前的体积之和为a,混合后总体积为b
查看习题详情和答案>>
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用水煤气合成二甲醚,其反应为:3H2(g)+3CO(g)  CH3OCH3(g)+CO2(g) ΔH<0
CH3OCH3(g)+CO2(g) ΔH<0
(1)在一定条件下的密闭容器中,该反应达到平衡后,只改变一个条件能同时提高反应速率和CO的转化率的是________(填字母代号,下同)。
a.降低温度 b.加入催化剂
c.缩小容器体积 d.减少CO2的浓度
(2)若反应在体积恒定的密闭容器中进行,下列能判断反应已达平衡状态的是________
a.3V正(CO2)=V逆(CO) b.生成a mol CO2的同时消耗3a mol H2
c.气体的密度不再改变 d.混合气体的平均相对分子质量不变
(3)300℃时,在体积为2L的容器中充入4 mol H2、6 mol CO。5min时,反应恰好达平衡,此时H2的转化率为75%。
① 5min时V(CO)=_________mol/(L·min)。该温度下,此反应的平衡常数为:_______
② 保持温度不变,在以上已达反应平衡的容器中,将每种物质同时增加1mol,则此时平衡将_______移动(填“正向”、“逆向”、“不”)
(4).下图中,甲装置为CH3OCH3、O2、KOH三者构成的燃烧电池,其电极均为Pt电极。装置乙中,C、D电极为Pb电极,其表面均覆盖着PbSO4,其电解液为稀H2SO4溶液。
① 写出甲装置中A极的电极反应式___________________________________________
② 写出乙装置中C极的电极反应式___________________________________________
③ 当有23克甲醚参加反应时,D电极的质量变化为______克。

查看习题详情和答案>>
某同学设计测定镀锌铁皮镀锌层厚度的实验方案:将单侧面积为S、质量为m1的镀锌
铁皮放入6mol·L-1的盐酸中,当气泡产生的速率显著减少时,取出铁片,用水冲洗,烘
干后称量,得到质量为m2,下列说法不正确的是
A.当铁片产生气泡速度减慢时,立即取出铁片,不冲洗就用酒精灯加热烘干,铁片可能继续和残留的盐酸反应,导致结果偏高
B.实验过程中产生气泡的速率是先慢,然后逐渐加快,再显著减慢,这是微电池和温度共同影响的结果
C.锌和铁在酸溶液中形成原电池,外电路中电流从铁流向锌
D.设锌镀层厚度为h,锌的密度为 ,那么
,那么
查看习题详情和答案>>
 ?aC(g)+2D(g)。达到平衡后,A物质的量浓度减小
?aC(g)+2D(g)。达到平衡后,A物质的量浓度减小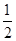 ,混合气体的平均摩尔质量增大
,混合气体的平均摩尔质量增大 ,则方程式中a值是
,则方程式中a值是