网址:http://m.1010jiajiao.com/timu3_id_148017[举报]
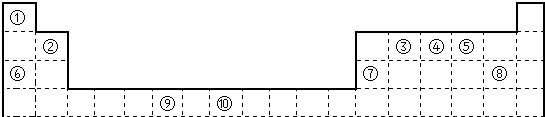
(用对应的元素符号回答下列问题)
(1)写出元素⑨的基态原子的价电子排布图




请利用电子排布的相关知识判断元素⑩形成的单核二价阳离子和单核三价阳离子较稳定的是
(2)①③⑤三种元素可以形成多种有机化合物分子,其中最简单原子数最少的一种是室内装潢时形成的主要气体污染物.试写出它的电子式
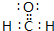
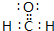
(3)元素④的氢化物的分子立体构型为
③④⑤三种元素的第一电离能大小关系是
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与氢氧化钠溶液反应的化学方程式:
(5)随着科学技术的发展,不断有新的元素被发现.若把第七周期排满,则元素周期表共可以排布
根据以下叙述和元素周期表的有关知识,回答下面试题:主族元素的性质主要由其原子的最外层电子数和电子层数决定,若元素的最外层电子数为m,电子层数为n,一般具有这样的规律:m>n的元素为非金属元素;m≤n的元素为金属元素。
6.下列有关结论正确的是( )
A.主族元素的性质随着原子量的递增而呈周期性变化
B.元素的金属性与非金属性递变规律最显著的是第三周期元素和第ⅣA族元素
C.ⅠA族和ⅦA族元素的单质一般都没有同素异形体
D.原子最外层电子数等于电子层数的元素均为金属元素
7.下列推断符合实际的有( )
A.第n周期的最后一种金属元素处在第n主族(n>1)
B.第n周期有8-n种非金属元素(n>1,包括稀有气体元素)
C.m=1和m=7的元素单质相互化合时,都形成离子化合物
D.m-n=5的主族元素存在最强的对应含氧酸;m-n=-5的元素对应的氧化物的水化物是最强的碱
查看习题详情和答案>>
(1)经验规律告诉我们:当形成化学键的两原子相应元素的x差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是________.
(2)根据上表给出的数据,简述主族元素的x的数值大小与元素的金属性或非金属性强弱之间的关系________________________________________.
(3)简述第二周期元素(除稀有气体外)的x的数值大小与原子半径之间的关系:__________________________.
(4)请你预测Br与I元素的x数值的大小关系:Br________I(填“>”、“=”或“<”).
(5)某有机化合物分子中含有S-N键,你认为该共用电子对偏向于________原子(填元素符号).
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出13种元素的X的数值:

试结合元素周期律知识完成下列问题:
(1)经验规律:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AIBr3中的化学键类型是________.
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系________.简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系________.
(3)某化合物分子中含有S-N键,该共用电子对偏向于________原子(填元素符号).
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质.下面给出14种元素的X的数值:

试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系________;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系________.
(3)某化合物分子中含有S-N键,你认为该共用电子对偏向于________原子(填元素符号).
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中的化学键类型是________.
(5)上表中元素形成的AB型化合物中,离子性最强的是________.