摘要:缓慢氧化:反应速率比较慢.不容易被人察觉的氧化反应.如:金属生锈.呼吸作用.食物腐败等. 自燃:由缓慢氧化放热引起的自发燃烧.
网址:http://m.1010jiajiao.com/timu3_id_140174[举报]
某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | 不加任何物质 | … |
| 2 | 2.0 | CuO 0.5 | … |
| 3 | 2.0 | MnO2 0.5 | … |
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
| 实验步骤 | 实验过程及现象 | 设计目的 |
| 1 | 加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 2 | CuO的质量在反应前后是否保持不变 | |
| 3 |
某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:
①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
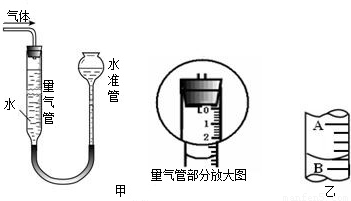
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
查看习题详情和答案>>

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | 不加任何物质 | … |
| 2 | 2.0 | CuO 0.5 | … |
| 3 | 2.0 | MnO2 0.5 | … |
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
| 实验步骤 | 实验过程及现象 | 设计目的 |
| 1 | 加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 2 | CuO的质量在反应前后是否保持不变 | |
| 3 |
查看习题详情和答案>>
某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
查看习题详情和答案>>

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | 不加任何物质 | … |
| 2 | 2.0 | CuO 0.5 | … |
| 3 | 2.0 | MnO2 0.5 | … |
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
| 实验步骤 | 实验过程及现象 | 设计目的 |
| 1 | 加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 2 | CuO的质量在反应前后是否保持不变 | |
| 3 |
查看习题详情和答案>>
某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
查看习题详情和答案>>

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | 不加任何物质 | … |
| 2 | 2.0 | CuO 0.5 | … |
| 3 | 2.0 | MnO2 0.5 | … |
(1)上述实验步骤中需要使用玻璃棒的是______(填序号).
(2)写出步骤③的化学方程式______.
(3)表格中的“待测数据”是指______.
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为______.
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
| 实验步骤 | 实验过程及现象 | 设计目的 |
| 1 | 加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 2 | CuO的质量在反应前后是否保持不变 | |
| 3 |
查看习题详情和答案>>
37、某研究性学习小组欲证明氧化铜也能作为氯酸钾分解反应的催化剂,他们进行了如下实验:

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是
(2)写出步骤③的化学方程式
(3)表格中的“待测数据”是指
(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为
(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
查看习题详情和答案>>

①称取1.0gCuSO4粉末加入10 mL蒸馏水完全溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚(一种可用于加热固体物质的容器)中,均匀缓慢加热至完全变为黑色的氧化铜,研细备用;
④按下表中的质量将固体混合好后,在相同条件下加热,并与MnO2的催化效果做比较,实验时间均以生成50 mL气体为准(见图甲),其他可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 其他物质质量(g) | 待测数据 |
| 1 | 2.0 | 不加任何物质 | … |
| 2 | 2.0 | CuO 0.5 | … |
| 3 | 2.0 | MnO2 0.5 | … |
(1)上述实验步骤中需要使用玻璃棒的是
①②③
(填序号).(2)写出步骤③的化学方程式
Cu(OH)2?CuO+H2O
.(3)表格中的“待测数据”是指
生成50mL气体所用的时间
.(4)若实验过程中50mL量气管中液面的位置如图乙所示,A与B刻度间相差1 mL,刻度A的读数为20,则此时量气管中收集到的气体体积为
20.80ml
.(5)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.
| 实验步骤 | 实验过程及现象 | 设计目的 |
| 1 | 加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 2 | CuO的质量在反应前后是否保持不变 | |
| 3 |