摘要:8.在(NH4)2SO4中氮元素的质量分数列式计算正确的是 ( ) (NH4)2SO4 (NH4)2SO4 A. 2N ×100% B. N×2 ×100% (NH4)2SO4 的相对分子质量 (NH4)2SO4 的质量 C. N的相对原子质量×2 ×100% D. N的相对原子质量×2 ×100%
网址:http://m.1010jiajiao.com/timu3_id_137580[举报]
在(NH4)2SO4中氮元素的质量分数列式计算正确的是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在(NH4)2SO4中氮元素的质量分数列式计算正确的是( )
查看习题详情和答案>>
A.
| ||
B.
| ||
C.
| ||
D.
|
肥田粉的主要成分是硫酸铵.现有一包标有含氮量为20.0%的肥田粉样品,小庆和小鸿为了计算该肥田粉中硫酸铵的质量分数,他们称取7.5g样品,分别采取下列方法:
小庆根据化学式计算:
解:硫酸铵中氮元素的质量分数:
×%
=
×%
=21.2%
设7.5g样品中含硫酸铵的质量为x.
x×21.2%=7.5g×20%
x=7.08g
样品中含硫酸铵的质量分数为:
×100%=94.4%
答:样品中含硫酸铵的质量分数为94.4%.
小鸿通过实验并根据化学方程式计算:
用称取的7.5g样品与足量的熟石灰混合加热,直到不再产生气体为止,得到纯净、干燥的氨气1.7g.该反应的化学方程式为:
(NH4)2SO4+Ca(0H)2
CaSO4+2NH↑+2H2O
(小鸿的计算过程由你来完成)
回答:
(1)请你根据小鸿的实验结果,计算样品中硫酸铵的质量分数.(结果精确到0.1%).
(2)你的计算结果和小庆的计算结果
(3)根据小鸿实验的反应原理分析,施用肥田粉时应注意
查看习题详情和答案>>
小庆根据化学式计算:
解:硫酸铵中氮元素的质量分数:
| N的相对原子质量×2 |
| (NH2)2SO4的相对分子质量 |
=
| 14×2 |
| 132 |
=21.2%
设7.5g样品中含硫酸铵的质量为x.
x×21.2%=7.5g×20%
x=7.08g
样品中含硫酸铵的质量分数为:
| 7.08g |
| 7.5g |
答:样品中含硫酸铵的质量分数为94.4%.
小鸿通过实验并根据化学方程式计算:
用称取的7.5g样品与足量的熟石灰混合加热,直到不再产生气体为止,得到纯净、干燥的氨气1.7g.该反应的化学方程式为:
(NH4)2SO4+Ca(0H)2
| ||
(小鸿的计算过程由你来完成)
回答:
(1)请你根据小鸿的实验结果,计算样品中硫酸铵的质量分数.(结果精确到0.1%).
(2)你的计算结果和小庆的计算结果
不同
不同
(填“相同”或“不同”),原因是小鸿在收集过程中部分氨气逸散
小鸿在收集过程中部分氨气逸散
.(3)根据小鸿实验的反应原理分析,施用肥田粉时应注意
不能与熟石灰等物质混合使用(合理即可)
不能与熟石灰等物质混合使用(合理即可)
.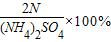
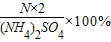
 ×100%
×100% 100%
100%

 ×100%
×100% 100%
100%