摘要:(1)① H2SO4 + BaCl2 = BaSO4↓ + 2HCl ② Ba(OH)2 + Na2SO4 = BaSO4↓ + 2NaOH (2)Ba2+ . SO42- K2SO4 + Ba(NO3)2 = BaSO4↓ + 2KNO3 (1分.其它合理答案均给分) 复分解反应
网址:http://m.1010jiajiao.com/timu3_id_133876[举报]
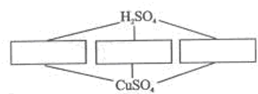 18、方框内是不同类别的物质,常温下与连线间的物质的溶液都能发生化学反应,如图所示:
18、方框内是不同类别的物质,常温下与连线间的物质的溶液都能发生化学反应,如图所示:(1)用化学式将不同类别的物质各一种写在方框内
(2)上述反应中不包含的化学反应基本类型的有
化合反应或分解反应
(填写一种)(3)写出有沉淀生产的中和反应
H2SO4+Ba(OH)2═BaSO4↓+2H2O
.(2013?和平区模拟)同学们通过以下在溶液中进行的实验,探究复分解反应发生的条件:
①H2SO4+Ba(NO3)2②H2SO4+NaOH ③H2SO4+Na2CO3 ④Ba(NO3)2+NaOH ⑤Ba(NO3)2+Na2CO3⑥NaOH+Na2CO3
(1)以上各组物质能够发生的是:
(2)同学们将实验后的所有物质倒入同一烧杯中,后续实验及现象如下
综合分析可知,无色滤液a中一定含有的溶质是
(3)下列有关利用无色滤液a和白色沉淀b的设想中,合理的是
A.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液a
B.制NaNO3溶液:向无色滤液a中加入适量的稀HNO3
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b
D.鉴别NH4Cl溶液和NaCl溶液:取样,滴加无色滤液a.
查看习题详情和答案>>
①H2SO4+Ba(NO3)2②H2SO4+NaOH ③H2SO4+Na2CO3 ④Ba(NO3)2+NaOH ⑤Ba(NO3)2+Na2CO3⑥NaOH+Na2CO3
(1)以上各组物质能够发生的是:
①②③⑤
①②③⑤
;(填序号)同学们总结归纳出复分解反应发生的条件是生成物中有沉淀,或气体,或水
沉淀,或气体,或水
;(2)同学们将实验后的所有物质倒入同一烧杯中,后续实验及现象如下

综合分析可知,无色滤液a中一定含有的溶质是
NaOH、NaNO3
NaOH、NaNO3
;可能含有的溶质是Na2SO4或Ba(NO3)2
Na2SO4或Ba(NO3)2
.白色沉淀b含有的物质有BaCO3、BaSO4
BaCO3、BaSO4
.(3)下列有关利用无色滤液a和白色沉淀b的设想中,合理的是
CD
CD
.A.鉴别MgCl2溶液和BaCl2溶液:取样,滴加无色滤液a
B.制NaNO3溶液:向无色滤液a中加入适量的稀HNO3
C.除去Ba(NO3)2溶液中的HNO3:向其中加入过量的白色沉淀b
D.鉴别NH4Cl溶液和NaCl溶液:取样,滴加无色滤液a.
(2009?杭州)实验室有两瓶标签脱落的溶液,只知道是盐酸溶液和硫酸溶液.请选择下列试剂:
①氧化铁②氢氧化钠溶液③碳酸钠溶液④氢氧化钡溶液⑤氯化钡溶液,用两种方法,每次只用一种试剂把它们鉴别出来.请填写下表:
查看习题详情和答案>>
①氧化铁②氢氧化钠溶液③碳酸钠溶液④氢氧化钡溶液⑤氯化钡溶液,用两种方法,每次只用一种试剂把它们鉴别出来.请填写下表:
| 选择的试剂编号 | 有明显反应现象的化学方程式 | |
| 方法一 | ④ ④ | H2SO4+Ba(OH)2=BaSO4↓+2H2O H2SO4+Ba(OH)2=BaSO4↓+2H2O |
| 方法二 | ⑤ ⑤ | H2SO4+BaCl2=2HCl+BaSO4↓ H2SO4+BaCl2=2HCl+BaSO4↓ |
下列各组物质,不用其他试剂,就可以加以鉴别的是( )
| A、CuSO4 KOH NaCl Na2SO4 | B、HCl(浓) Na2CO3 BaCl2 Na2SO4 | C、H2SO4 Ba(OH)2 KNO3 NaCl | D、NaOH HCl NaCl KNO3 |
(2011?杨浦区二模)写出下列反应的化学方程式:
(1)木炭在氧气中充分燃烧生成二氧化碳
(2)在加热条件下氢气和氧化铜反应生成铜和水
(3)稀硫酸和硝酸钡溶液反应
(4)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为
(5)金属镁着火不能用CO2灭火,请用化学方程式表示其原因
(6)用“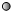 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为:
”表示氧原子,则如图所示的化学反应方程式为:
(7)写出用CaCO3、H2O、Na2CO3为原料制取NaOH的各步反应的方程式:
第一步:分解反应
第二步:化合反应
第三步:复分解反应
查看习题详情和答案>>
(1)木炭在氧气中充分燃烧生成二氧化碳
C+O2
CO2
| ||
C+O2
CO2
;
| ||
(2)在加热条件下氢气和氧化铜反应生成铜和水
H2+CuO
Cu+H2O
| ||
H2+CuO
Cu+H2O
;
| ||
(3)稀硫酸和硝酸钡溶液反应
H2SO4+Ba(NO3)2=BaSO4↓+2HNO3
H2SO4+Ba(NO3)2=BaSO4↓+2HNO3
.(4)用CO高温下还原赤铁矿(主要成份Fe2O3)的化学方程式为
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
.
| ||
(5)金属镁着火不能用CO2灭火,请用化学方程式表示其原因
2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
,反应基本类型是
| ||
置换反应
置换反应
.(6)用“
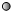 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则如图所示的化学反应方程式为:
”表示氧原子,则如图所示的化学反应方程式为:2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||

(7)写出用CaCO3、H2O、Na2CO3为原料制取NaOH的各步反应的方程式:
第一步:分解反应
CaCO3
CaO+CO2↑
| ||
CaCO3
CaO+CO2↑
;
| ||
第二步:化合反应
CaO+H2O=Ca(OH)2
CaO+H2O=Ca(OH)2
;第三步:复分解反应
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
Ca(OH)2+Na2CO3=2NaOH+CaCO3↓
.