摘要:工业上用电解氯化镁方法生产金属镁:MgCl2 ===== Mg + Cl2↑.现电解950Kg氯化镁最多能生产多千克单质镁?同时能得到多少千克氯气? 答案 课题3 1.BD 解析:三种物质发生的是化合反应.A+B+C→D .则“增加10 g A.则反应停止后.原反应物中只余C .说明A与B恰好完全反应时的质量比为25:5=5:3.则在第一次反应中.反应掉的A与B的质量分别是15g和6g.由于生成D的质量是30g.故参加反应的C的质量为:30g-15g-9g=6g.即完全反应时A.B.C.D四种物质的质量比为:15:9:6:30.则第二次反应掉的C是10g,生成的D是50g.故A.C错.B.D对. 点评:本题要充分利用质量守恒定律和反应过程中各物质的质量成比例来分析.2.C 解析:镁燃烧是镁与空气中的氧气发生了化合反应:2Mg + O2 点燃 2MgO 则氧化镁的质量等于参加反应的镁和氧气的质量和.点评:本题考察学生对质量守恒定律的理解.物质在空气中的燃烧.一定有氧气参加.故反应物的质量是可燃物与氧气的质量和.3.B 4.解法:设可制得氢气的质量为X. Zn+H2SO4==ZnSO4+H2↑ 65 2
网址:http://m.1010jiajiao.com/timu3_id_127669[举报]
 Mg+Cl2↑.现电解190Kg氯化镁最多能生产多千克单质镁?
Mg+Cl2↑.现电解190Kg氯化镁最多能生产多千克单质镁?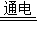 Mg+Cl2↑.
Mg+Cl2↑.