摘要:金属钠与盐酸的反应:
网址:http://m.1010jiajiao.com/timu3_id_126103[举报]
酸的性质是(写出有关的化学方程式)
(1)酸溶液能与酸碱指示剂反应,使 试液变红,使 试液不变色.
(2)酸+活泼金属→ + . 例:铁和稀盐酸反应 .
(3)酸+金属氧化物→ + .例:氧化铁和稀硫酸反应 .
(4)酸+碱→ + .例:盐酸和氢氧化钠反应 .
(5)酸+碳酸盐→二氧化碳 例:碳酸钙和稀盐酸反应 .
查看习题详情和答案>>
(1)酸溶液能与酸碱指示剂反应,使
(2)酸+活泼金属→
(3)酸+金属氧化物→
(4)酸+碱→
(5)酸+碳酸盐→二氧化碳 例:碳酸钙和稀盐酸反应
金属材料在生活、生产中应用十分广泛.
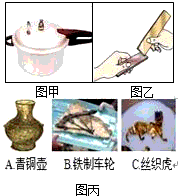
(1)图甲是金属的一个应用实例,利用了金属的________性.
(2)图乙是纯铜片与铜合金片两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是________.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图丙是古船上的一些文物图片.
Ⅰ.图丙中出土文物不属于合金的是________.
Ⅱ.考古人员还惊喜地在一个铜壶中发现了特殊的液体,闻起来有一股酒香味.
①小明从微粒性质的角度分析,能闻到酒香味,说明________.
②为证明这种液体是酒,有人提出下面三种方法,你认为较科学的是________(填序号).
A、喝一口品尝B、使用酒精测试仪测试C、将其点燃
Ⅲ.【请你分析】:为什么出土的青铜器保存较好,而铁器却锈蚀严重?
________.
(4)已知某合金粉末的成份除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.下面请你和他们一起探究:
【查阅资料】:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】:猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有________.(填名称)
猜想3:该合金粉末中除铝外,还含有铁和铜.
【实验探究】:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的________,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出 | 合金中一定含有________ |
| ②取步骤①所得滤渣,加过量的________,充分反应 | 滤渣又部分溶解也有气体放出. | 合金中一定含有________ |
【拓展探究】:某学生还想进一步验证铝、铁、铜三种金属的活动性顺序,他设计了以下四种实验方案,其中能够达到实验目的有________
A.将Al、Cu分别加入到FeSO4溶液中;B.将Al、Fe分别加入到CuSO4溶液中
C.将Al分别加入到FeSO4、CuSO4溶液中;D.将Fe分别加入到Al2(SO4)3、CuSO4溶液. 查看习题详情和答案>>
金属铝是一种比较特殊的金属,不仅能与稀盐酸反应产生氢气,还能与氢氧化钠溶液反应产生氢气.其反应化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.现反应产生3g H2,则参加反应的NaOH的质量为多少克?
查看习题详情和答案>>金属材料在生活、生产中应用十分广泛.

(1)图甲是金属的一个应用实例,利用了金属的_________.
(2)图乙是纯铜片与铜合金片两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是_________.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图丙是古船上的一些文物图片.
Ⅰ.图丙中出土文物不属于合金的是_________.
Ⅱ.考古人员还惊喜地在一个铜壶中发现了特殊的液体,闻起来有一股酒香味.
①小明从微粒性质的角度分析,能闻到酒香味,说明_________.
②为证明这种液体是酒,有人提出下面三种方法,你认为较科学的是_________(填序号).A、喝一口品尝B、使用酒精测试仪测试C、将其点燃
Ⅲ.【请你分析】为什么出土的青铜器保存较好,而铁器却锈蚀严重?_________.
(4)已知某合金粉末的成份除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.下面请你和他们一起探究:
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O==2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】猜想1:该合金粉末中除铝外,还含有铁.猜想2:该合金粉末中除铝外,还含有_________.(填名称)猜想3:该合金粉末中除铝外,还含有铁和铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
(2)图乙是纯铜片与铜合金片两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是_________.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图丙是古船上的一些文物图片.
Ⅰ.图丙中出土文物不属于合金的是_________.
Ⅱ.考古人员还惊喜地在一个铜壶中发现了特殊的液体,闻起来有一股酒香味.
①小明从微粒性质的角度分析,能闻到酒香味,说明_________.
②为证明这种液体是酒,有人提出下面三种方法,你认为较科学的是_________(填序号).A、喝一口品尝B、使用酒精测试仪测试C、将其点燃
Ⅲ.【请你分析】为什么出土的青铜器保存较好,而铁器却锈蚀严重?_________.
(4)已知某合金粉末的成份除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.下面请你和他们一起探究:
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O==2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】猜想1:该合金粉末中除铝外,还含有铁.猜想2:该合金粉末中除铝外,还含有_________.(填名称)猜想3:该合金粉末中除铝外,还含有铁和铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.

【探究结论】猜想3成立.
【拓展探究】某学生还想进一步验证铝、铁、铜三种金属的活动性顺序,他设计了以下四种实验方案,其中能够达到实验目的有_________
A.将Al、Cu分别加入到FeSO4溶液中;
B.将Al、Fe分别加入到CuSO4溶液中
C.将Al分别加入到FeSO4、CuSO4溶液中;
D.将Fe分别加入到Al2(SO4)3、CuSO4溶液.
查看习题详情和答案>>
【拓展探究】某学生还想进一步验证铝、铁、铜三种金属的活动性顺序,他设计了以下四种实验方案,其中能够达到实验目的有_________
A.将Al、Cu分别加入到FeSO4溶液中;
B.将Al、Fe分别加入到CuSO4溶液中
C.将Al分别加入到FeSO4、CuSO4溶液中;
D.将Fe分别加入到Al2(SO4)3、CuSO4溶液.
金属材料在生活、生产中应用十分广泛.
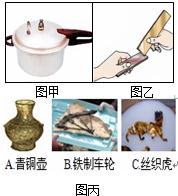
(1)图甲是金属的一个应用实例,利用了金属的______性.
(2)图乙是纯铜片与铜合金片两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是______.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图丙是古船上的一些文物图片.
Ⅰ.图丙中出土文物不属于合金的是______.
Ⅱ.考古人员还惊喜地在一个铜壶中发现了特殊的液体,闻起来有一股酒香味.
①小明从微粒性质的角度分析,能闻到酒香味,说明______.
②为证明这种液体是酒,有人提出下面三种方法,你认为较科学的是______(填序号).
A、喝一口品尝B、使用酒精测试仪测试C、将其点燃
Ⅲ.【请你分析】:为什么出土的青铜器保存较好,而铁器却锈蚀严重?
______.
(4)已知某合金粉末的成份除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.下面请你和他们一起探究:
【查阅资料】:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】:猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有______.(填名称)
猜想3:该合金粉末中除铝外,还含有铁和铜.
【实验探究】:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
【探究结论】:猜想3成立.
【拓展探究】:某学生还想进一步验证铝、铁、铜三种金属的活动性顺序,他设计了以下四种实验方案,其中能够达到实验目的有______
A.将Al、Cu分别加入到FeSO4溶液中;B.将Al、Fe分别加入到CuSO4溶液中
C.将Al分别加入到FeSO4、CuSO4溶液中;D.将Fe分别加入到Al2(SO4)3、CuSO4溶液.
查看习题详情和答案>>

(1)图甲是金属的一个应用实例,利用了金属的______性.
(2)图乙是纯铜片与铜合金片两块金属片相互刻划后,在纯铜片上有明显的划痕.该实验探究的目的是______.
(3)2007年12月,南宋古沉船“南海一号”成功打捞出水.图丙是古船上的一些文物图片.
Ⅰ.图丙中出土文物不属于合金的是______.
Ⅱ.考古人员还惊喜地在一个铜壶中发现了特殊的液体,闻起来有一股酒香味.
①小明从微粒性质的角度分析,能闻到酒香味,说明______.
②为证明这种液体是酒,有人提出下面三种方法,你认为较科学的是______(填序号).
A、喝一口品尝B、使用酒精测试仪测试C、将其点燃
Ⅲ.【请你分析】:为什么出土的青铜器保存较好,而铁器却锈蚀严重?
______.
(4)已知某合金粉末的成份除铝外,还含有铁、铜中的一种或两种.某化学兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.下面请你和他们一起探究:
【查阅资料】:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】:猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有______.(填名称)
猜想3:该合金粉末中除铝外,还含有铁和铜.
【实验探究】:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的______,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出 | 合金中一定含有______ |
| ②取步骤①所得滤渣,加过量的______,充分反应 | 滤渣又部分溶解也有气体放出. | 合金中一定含有______ |
【拓展探究】:某学生还想进一步验证铝、铁、铜三种金属的活动性顺序,他设计了以下四种实验方案,其中能够达到实验目的有______
A.将Al、Cu分别加入到FeSO4溶液中;B.将Al、Fe分别加入到CuSO4溶液中
C.将Al分别加入到FeSO4、CuSO4溶液中;D.将Fe分别加入到Al2(SO4)3、CuSO4溶液.