摘要:有一个选项符合题意.请将正确选项的字母填写在右边的括 号内.)1.近来很多城市部分居民首次用上了由“西气东输 管道送来的天然气.天然气的主要成分 是 ( ) A.氢气 B.一氧化碳 C.甲烷 D.乙醇
网址:http://m.1010jiajiao.com/timu3_id_124930[举报]
每小题只有一个选项符合题意,请将符合题阅读下列资料,回答下列各题
久早不雨,地面严重缺水时,人们常用人造雨的技术增加降雨量.造雨的方法随云的性质而不同:在0℃以上的暖云内可撒播盐粒,盐粒会吸收水分,使其周围的小水滴向它靠拢,最后成为雨滴掉下来;在0℃以下的冷云中可撒播干冰,干冰会使周围空气的温度急剧下降,以致云中的水气或水滴迅速冻结成冰晶,最后形成雨滴降落地面.此外也可使用碘化银,碘化银的蒸气在0℃以下的云层中会形成微粒,产生类似前述冰晶的效果.
(1).根据选文中的资料,在人造雨的作业中,不适合使用下列哪一种物质( )
A.液态碳氢化合物(![]() )
)
B.固态二氧化碳(![]() )
)
C.氯化钠(NaCl)晶体
D.碘化银(AgI)晶体
(2).根据选文的资料,目前人造雨技术所应用的原理是:( )
A.使云中的小水滴凝聚成大水滴
B.促使地面水分蒸发以增加云量
C.使云的高度上升以降低其温度
D.将云块驱赶到集水区域的上空
查看习题详情和答案>>
选择题(下题有1~2个选项符合题意)有关水的组成的下列说法中正确的是
- A.由氢分子和氧原子构成
- B.由二个氢元素和一个氧元素组成
- C.由氢气和氧气按2∶1体积比混合而成
- D.由氢元素和氧元素组成
如图1是实验室常用的装置.请据图回答:
(1)写出仪器①的名称
(2)用高锰酸钾制取氧气的装置组合是
(3)实验室制得的CO2气体中常含有HCl和水蒸气.为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是
A.a→b→c→d B.b→a→c→d C.c→d→a→b D.d→c→b→a
(4)CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如图2实验装置.请回答以下有关问题:
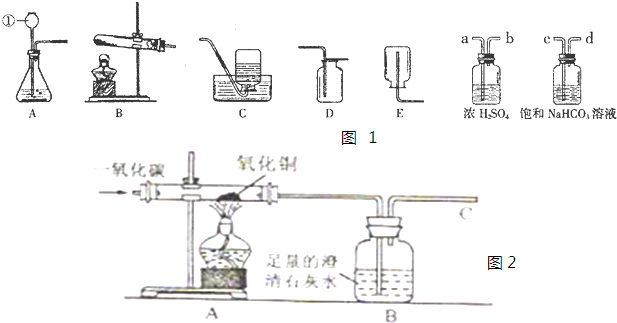
①实验开始时,先通人CO一段时间后,再加热,其原因是
②实验中图A处玻璃管中发生的现象是
③该装置中有一个明显的缺陷,请指出改正方法
查看习题详情和答案>>
(1)写出仪器①的名称
长颈漏斗
长颈漏斗
.收集某气体只能采用E装置,由此推测该气体具有的性质易溶于水,密度比空气的密度
易溶于水,密度比空气的密度
;(2)用高锰酸钾制取氧气的装置组合是
BC或BD;
BC或BD;
(填序号),反应的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
;
| ||
(3)实验室制得的CO2气体中常含有HCl和水蒸气.为了得到纯净、干燥的CO2气体,除杂装置的导管气流方向连接顺序是
C
C
(填选项).A.a→b→c→d B.b→a→c→d C.c→d→a→b D.d→c→b→a
(4)CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如图2实验装置.请回答以下有关问题:

①实验开始时,先通人CO一段时间后,再加热,其原因是
排尽装置内的空气,防止加热时发生爆炸
排尽装置内的空气,防止加热时发生爆炸
②实验中图A处玻璃管中发生的现象是
粉末由黑色逐渐变成红色
粉末由黑色逐渐变成红色
,其化学反应方程式为CuO+CO
Cu+CO2
| ||
CuO+CO
Cu+CO2
| ||
③该装置中有一个明显的缺陷,请指出改正方法
在C处加一个尾气处理装置
在C处加一个尾气处理装置
. CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:
CO是一种无色、无味、有毒的可燃气体污染物,具有还原性,可用于冶金工业.某兴趣小组为探究其具有还原性,设计了如下实验装置.请回答以下有关问题:①实验开始时,先通入CO一段时间后,再加热,其原因是
先通入一氧化碳,将玻璃管内的空气排干净,以免一氧化碳气体和氧气混合,遇到明火可能会发生爆炸
先通入一氧化碳,将玻璃管内的空气排干净,以免一氧化碳气体和氧气混合,遇到明火可能会发生爆炸
②实验中图A处玻璃管中发生的现象是
反应物由黑色变成红色
反应物由黑色变成红色
,其化学反应方程式为CO+CuO
Cu+CO2
| ||
CO+CuO
Cu+CO2
| ||
③该装置中有一个明显的缺陷,请指出改正方法
没有尾气处理装置,在连接试管的导管出口处接一个气球将气体收集起来或放一盏燃着的酒精灯,将尾气燃烧掉
没有尾气处理装置,在连接试管的导管出口处接一个气球将气体收集起来或放一盏燃着的酒精灯,将尾气燃烧掉
④实验改正后B图导管出口处反应发生的现象是
有蓝色火焰产生
有蓝色火焰产生
其化学反应方程式为2CO+O2
2CO2
| ||
2CO+O2
2CO2
.
| ||
 23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.
23、某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究.请你参与他们的探究活动,并回答有关问题.(1)查阅资料:①SO2常温下是一种无色气体,易溶于水;②酸能使蓝色石蕊试纸变成红色;③SO2有毒.
(2)提出假设:SO2能与H2O反应生成酸.
(3)实验探究:设计如右图所示装置进行实验.
①实验过程中,A装置内蓝色石蕊试纸的颜色始终没有变化.A装置的作用是
证明SO2不能使蓝色石蕊试纸变色
.②在通入SO2之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,此步操作的目的是
证明水不能使蓝色石蕊试纸变色
.当有SO2通过时发现湿润的蓝色石蕊试纸变红,此现象说明
SO2与水反应生成酸
,此过程中反应的化学方程式为
SO2+H2O=H2SO3
.(4)结论:原假设成立.
(5)反思与评价:该实验方案中,有一个明显的疏漏,请你帮他们指出不足之处
尾气没有处理
.(6)拓展探究:该研究性学习小组取刚降到硫酸厂(生产过程中产生SO2)附近的雨水进行测定,每隔几分钟测一次pH,其数据如下表所示:

分析上述数据的变化,你可得出的结论是
随着时间的变化,雨水的酸性逐渐增强
;针对此结论,你猜测其中的原因为
H2SO3与空气中的O2反应生成了H2SO4
.结合大理石雕像受到酸雨腐蚀的事实,你认为碳酸、硫酸、亚硫酸(H2SO3)酸性由强到弱的顺序是
H2SO4>H2SO3>H2CO3
.