摘要:11.下列有关叙述错误的是 A.若根据反应“H2+Cl2=2HCl 设计成燃料电池.既可发电同时还可用于工业制盐酸 B.冰醋酸中逐滴加水.则溶液的导电性和醋酸的电离程度均先增大后减小 C.某反应△H>0.△S>0.该反应可能自发进行 D.25℃时.NaClO溶液的pH=8.c(Na-)-c()=9.9×10-7mol/L.
网址:http://m.1010jiajiao.com/timu3_id_1247211[举报]
下列有关叙述错误的是
A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸
B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
C.某反应△H>0,△S>0,该反应可能自发进行
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(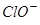 )=9.9×10-7mol/L.
)=9.9×10-7mol/L.
查看习题详情和答案>>
下列有关叙述错误的是
A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸
B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
C.某反应△H>0,△S>0,该反应可能自发进行
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(![]() )=9.9×10-7mol/L.
)=9.9×10-7mol/L.
下列有关叙述错误的是
A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸
B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小
C.某反应△H>0,△S>0,该反应可能自发进行
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(![]() )=9.9×10-7mol/L.
)=9.9×10-7mol/L.
查看习题详情和答案>>
下列有关叙述错误的是
| A.若根据反应“H2+Cl2=2HCl”设计成燃料电池,既可发电同时还可用于工业制盐酸 |
| B.冰醋酸中逐滴加水,则溶液的导电性和醋酸的电离程度均先增大后减小 |
| C.某反应△H>0,△S>0,该反应可能自发进行 |
D.25℃时,NaClO溶液的pH=8,c(Na-)—c(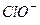 )=9.9×10-7mol/L. )=9.9×10-7mol/L. |
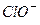 )=9.9×10-7mol/L.
)=9.9×10-7mol/L.