摘要:28.向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸.请回答相关问题: ①当加入10.00mL盐酸时.溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c( )>c( )>c( )>c( ) ②当盐酸与氨水等物质的量反应时.溶液的pH 7(填“> 或“< 或“= .下同) ③当溶液pH=7时.反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n(NH3·H2O) n(HCl).溶液中c( NH4+) c(Cl-). (2)已知某弱酸的酸式酸根离子HB-既能发生电离.又能发生水解.请通过实验确定HB-离子是电离程度大还是水解程度大?请简述实验过程和结论.
网址:http://m.1010jiajiao.com/timu3_id_1243108[举报]
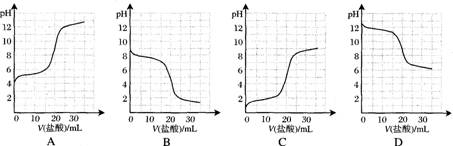
(1)向20.00mL稀氨水中逐滴加入等物质的量浓度的盐酸,请回答相关问题:
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c______>c______>c______>c______
②当盐酸与氨水等物质的量反应时,溶液的pH______7(填“>”或“<”或“=”,下同)
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n(NH3?H2O)______n(HCl),溶液中c( NH4+)______c(Cl-).
(2)已知某弱酸的酸式酸根离子HB-既能发生电离,又能发生水解,请通过实验确定HB-离子是电离程度大还是水解程度大?请简述实验过程和结论.____________.
查看习题详情和答案>>
①当加入10.00mL盐酸时,溶液中各种离子浓度之间的大小关系为(请在括号中填入离子符号):c______>c______>c______>c______
②当盐酸与氨水等物质的量反应时,溶液的pH______7(填“>”或“<”或“=”,下同)
③当溶液pH=7时,反应所消耗的物质(包括还在溶液中存留的物质)之间的关系为:n(NH3?H2O)______n(HCl),溶液中c( NH4+)______c(Cl-).
(2)已知某弱酸的酸式酸根离子HB-既能发生电离,又能发生水解,请通过实验确定HB-离子是电离程度大还是水解程度大?请简述实验过程和结论.____________.