摘要:如图是某研究小组利用实验室制氯气的装置设计制取氯水并进行相关实验. (1)A装置中发生化学反应的离子方程式为 . (2)氯气能使湿润的红色布条褪色.对于使红色布条褪色的物质.同学们的看法不一致.认为氯水中存在的几种粒子都有可能.请你设计实验.得出正确结论. ①提出假设 假设一 . 假设二 . 假设三 . 假设四 H2O使布条褪色 ②设计实验方案 基于提出的假设.设计出实验方案 ③实验过程 实验①: , 实验②: . 实验③:把红色布条放在水里.布条不褪色. ④得出结论 . (3)用量筒取20mL氯水.倒入已检查完好的分液漏斗中.然后再注入10mL CCl4.盖好玻璃塞.振荡.静置分层,呈黄绿色的是 (填“上层液 或“下层液 ).能使有色布条褪色的是 (填“上层液 或“下层液 ) (4)这套装置的缺点是 .如何改进.在右框中画出改进的实验装置图.
网址:http://m.1010jiajiao.com/timu3_id_1236577[举报]
如图是某研究性学习小组设计的几种装置,请你分析并回答下列问题:

(1)图中标号仪器为:a
(2)用氯酸钾制取氧气时的发生装置应选
a.烘干 b.溶解 c.过滤 d.洗涤
(3)小勤同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,则与A相比,B的优点是
(4)在实验室用装置C制取CO2的化学反应方程式为
查看习题详情和答案>>

(1)图中标号仪器为:a
铁架台
铁架台
.(2)用氯酸钾制取氧气时的发生装置应选
D
D
,反应的化学方程式为:2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
.对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应),通过以下四步实验操作可回收二氧化锰.正确操作的先后顺序是
| ||
| △ |
b c d a
b c d a
(填写选项序号). a.烘干 b.溶解 c.过滤 d.洗涤
(3)小勤同学从装置A得到启发,在装置A的基础上增加了隔离铜网改成装置B来制取氢气,则与A相比,B的优点是
可控制反应的发生和停止
可控制反应的发生和停止
,而装置B显示的反应为已停止
已停止
(填“进行中”或“已停止”),小明用一支底部有一个小洞的试管和矿泉水瓶组合成装置C(夹持仪器都略去),C与B相比不同之是废物利用
废物利用
(从资源角度考虑).(4)在实验室用装置C制取CO2的化学反应方程式为
CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
,若CO2中含有水蒸气,须将气体装置F以除去水蒸气,则F中的溶液名称是浓硫酸
浓硫酸
,气体应从m
m
(填字母)口进入.
某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空.
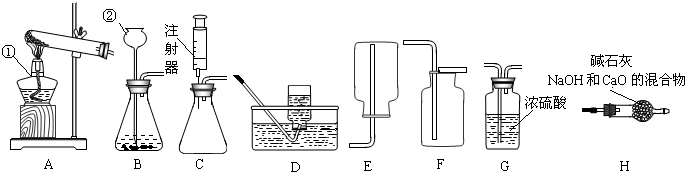
(1)写出图中有标号仪器的名称:① 、② ;
(2)用双氧水和二氧化锰来制取氧气时,可选用的最佳装置组合是 (填序号),其中二氧化锰起 作用.
(3)实验用氯酸钾制取氧气时,发生反应的化学方程式为 .
(4)上述两种制氧气的方法,最好选方法(2)的原因是(至少1点) .
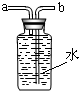
(5)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是 ;如果用如图所示装置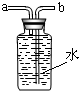 收集乙炔,气体应从 (填“a”或“b”)端管口通入.
收集乙炔,气体应从 (填“a”或“b”)端管口通入.
(6)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性;氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.
①制取并收集一瓶干燥氨气的装置连接顺序为 (填标号).
②小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是 , .
查看习题详情和答案>>

(1)写出图中有标号仪器的名称:①
(2)用双氧水和二氧化锰来制取氧气时,可选用的最佳装置组合是
(3)实验用氯酸钾制取氧气时,发生反应的化学方程式为
(4)上述两种制氧气的方法,最好选方法(2)的原因是(至少1点)
(5)实验室在常温下用块状电石与水反应制取微溶于水的乙炔气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂.你认为上图中最适合制取乙炔气体的发生装置是
 收集乙炔,气体应从
收集乙炔,气体应从(6)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性;氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体.
①制取并收集一瓶干燥氨气的装置连接顺序为
②小芳将收集满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是
某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空.

(1)写出图中仪器a.b的名称 a
(2)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是
(3)小陈同学选用图1装置做硫在氧气中燃烧的实验,请仔细观察,该同学的实验造成后果是
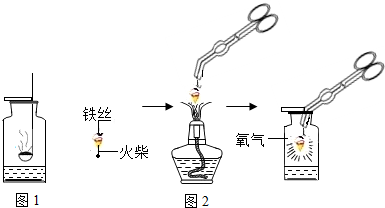
(4)小吴同学用制取的氧气,进行细铁丝在氧气中燃烧的性质实验.
①写出细铁丝在氧气中化学方程式:
②图2中螺旋状铁丝的末端系一根火柴的作用是
③小吴按图2实验时,发现铁丝没有燃烧,可能的原因有
(5)乙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2
做出上述猜想的理由是
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变.则猜想
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
查看习题详情和答案>>

(1)写出图中仪器a.b的名称 a
试管
试管
,b集气瓶
集气瓶
.(2)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
,应选择的发生装置是
| ||
| △ |
A
A
,收集氧气的一种装置是C或D
C或D
(填字母),理由是氧气不易溶于水或氧气的密度比空气的密度大
氧气不易溶于水或氧气的密度比空气的密度大
;(3)小陈同学选用图1装置做硫在氧气中燃烧的实验,请仔细观察,该同学的实验造成后果是
污染空气
污染空气
;
(4)小吴同学用制取的氧气,进行细铁丝在氧气中燃烧的性质实验.
①写出细铁丝在氧气中化学方程式:
3Fe+2O2
Fe3O4
| ||
3Fe+2O2
Fe3O4
| ||
②图2中螺旋状铁丝的末端系一根火柴的作用是
引燃铁丝
引燃铁丝
.③小吴按图2实验时,发现铁丝没有燃烧,可能的原因有
集气瓶中氧气的含量低
集气瓶中氧气的含量低
(只填一种).(5)乙同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,该反应的化学方程式为
2KMnO4
K2MnO4+MnO2+O2↑
| ||
2KMnO4
K2MnO4+MnO2+O2↑
.实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
| ||
【提出猜想】猜想Ⅰ:反应生成的MnO2分解放出O2;
猜想Ⅱ:反应生成的K2MnO4分解放出O2
做出上述猜想的理由是
二氧化锰和锰酸钾中都含有氧元素
二氧化锰和锰酸钾中都含有氧元素
.【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变.则猜想
Ⅰ
Ⅰ
错误.②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法得出了猜想Ⅱ正确的结论.该组同学选择的实验方法是
将生成物通入水中,发现有气泡生成
将生成物通入水中,发现有气泡生成
.
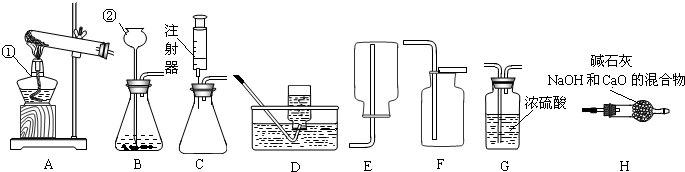
 收集乙炔,气体应从______(填“a”或“b”)端管口通入.
收集乙炔,气体应从______(填“a”或“b”)端管口通入.