网址:http://m.1010jiajiao.com/timu3_id_1234623[举报]
 某化学反应中,设反应物的总能量为E1,生成物的总能量为E2.
某化学反应中,设反应物的总能量为E1,生成物的总能量为E2.
(1)若E1>E2,则该反应为
(2)若E1<E2,则该反应为
(3)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热/KJ?mol-1 | 参考价格/元?kg-1 |
| CaCL2?6H2O | 29,0 | 37,3 | 780~850 |
| Na2SO4?10H2O | 32,4 | 77,0 | 800~900 |
| Na2HPO4?12H2O | 36,1 | 100,1 | 1600~2000 |
| Na2S2O3?5H2O | 48,5 | 49,7 | 1400~1800 |
A.CaCL2?6H2O B、Na2SO4?10H2O C.Na2HPO4?12H2O D、Na2S2O3?5H2O
②右图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据对水的密度的认识,你估计在阳光照射下水将沿
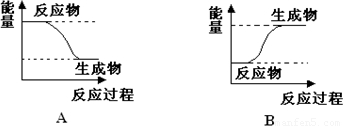
(1)若E1>E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(2)若E1<E2,则该反应为 (填“放热”或“吸热”)反应.该反应可用图 (填“A”或“B”)表示.
(3)太阳能的开发和利用是21世纪的一个重要课题.
①利用储能介质储存太阳能的原理是白天在太阳照射下,某种盐熔化,吸收热量;晚间熔盐释放出相应能量,从而使室温得以调节.已知下列数据:
| 盐 | 熔点/℃ | 熔化吸热/KJ?mol-1 | 参考价格/元?kg-1 |
| CaCL2?6H2O | 29,0 | 37,3 | 780~850 |
| Na2SO4?10H2O | 32,4 | 77,0 | 800~900 |
| Na2HPO4?12H2O | 36,1 | 100,1 | 1600~2000 |
| Na2S2O3?5H2O | 48,5 | 49,7 | 1400~1800 |
A.CaCL2?6H2O B、Na2SO4?10H2O C.Na2HPO4?12H2O D、Na2S2O3?5H2O
②右图是一种太阳能热水器的示意图,图中A是集热器,B是储水容器,C是供阴天时加热的辅助电热器.根据对水的密度的认识,你估计在阳光照射下水将沿 (填“顺”或“逆”)时针方向流动.
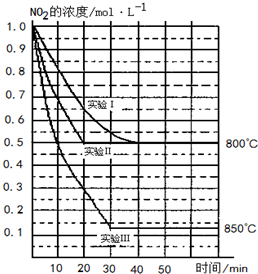 某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)
某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol?L-1)随时间(min)的变化如图所示.请回答下列问题:
在2L密闭容器内,800℃时反应:2NO2(g)?2NO(g)+O2(g)体系中,n(NO2)随时间的变化如表:
(1)实验Ⅱ隐含的反应条件是
(2)写出该反应的平衡常数表达式:K=
| c(NO)2×c(O2) |
| c(NO2)2 |
| c(NO)2×c(O2) |
| c(NO2)2 |
(3)若实验Ⅰ中达平衡后,再向密闭容器中通入2mol由物质的量之比为1:1组成的NO2与O2混合气体(保持温度不变),则平衡将
(4)若将上述第(3)题所得的平衡混和气体通入足量的NaOH溶液中,使气体被充分吸收.生成的产物及其物质的量为
(5)NO2、NO是重要的大气污染物,近年来人们利用NH3在一定条件下与之反应而将其转化为无害的参与大气循环的物质,该反应的化学方程式为
(12分)工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g)CH3OH(g) ΔH =-akJ·mol-1
(1)上图是该反应在不同温度下CO的转化率随时间变化的曲线。
① a __0(填“>” “<” “=”)。
② 下列说法正确的是_ _(填序号)。
a.1 molCO(g) 和2 mol H2(g) 所具有的能量小于1 mol CH3OH(g) 所具有的能量
b.将1 molCO(g) 和2 mol H2(g) 置于一密闭容器中充分反应后放出a KJ的热量
c.升高温度,平衡向逆反应移动,上述热化学方程式中的a值将减小
d.如将一定量CO(g) 和H2(g)置于某密闭容器中充分反应后放热a KJ,则此过程中有1 mol CO(g) 被还原
(2)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示:
① 该合成路线对于环境保护的价值在于_ _。
② 15%~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2
吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
。
(3)甲醇燃料电池的工作原理如下左图所示。该电池工作时,c口通入的物质发生的电极
反应式为:_ _。
(4)以上述电池做电源,用上右图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
_ 。
查看习题详情和答案>>
(12分)工业上一般可采用如下反应来合成甲醇:
CO(g)+2H2(g) CH3OH(g)
ΔH =-a
kJ·mol-1
CH3OH(g)
ΔH =-a
kJ·mol-1

(1)上图是该反应在不同温度下CO的转化率随时间变化的曲线。
① a __0(填“>” “<” “=”)。
② 下列说法正确的是_ _(填序号)。
a.1 mol CO(g) 和2 mol H2(g) 所具有的能量小于1 mol CH3OH(g) 所具有的能量
b.将1 mol CO(g) 和2 mol H2(g) 置于一密闭容器中充分反应后放出a KJ的热量
c.升高温度,平衡向逆反应移动,上述热化学方程式中的a值将减小
d.如将一定量CO(g) 和H2(g) 置于某密闭容器中充分反应后放热a KJ,则此过程中有1 mol CO(g) 被还原
(2)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示:

① 该合成路线对于环境保护的价值在于_ _。
② 15%~20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2
吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因:
。
(3)甲醇燃料电池的工作原理如下左图所示。该电池工作时,c口通入的物质发生的电极
反应式为:_ _。

(4)以上述电池做电源,用上右图所示装置,在实验室中模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示):
_ 。
查看习题详情和答案>>