摘要:小 大 左
网址:http://m.1010jiajiao.com/timu3_id_123384[举报]
小丽在观察课本实验“燃烧的条件”(左图)时,经查阅资料知产生的大量白烟对人体健康有影响,于是对此实验进行改进(右图),将足量的红磷和白磷分别放于两个大试管中,用橡皮塞塞好,然后将两大试管同时浸在盛有80℃热水的烧杯中.(着火点:白磷为40℃、红磷为240℃)
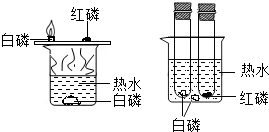
(1)试管内可观察到的现象为 由此得出可燃物燃烧必须具备的条件是 .
(2)改进后的装置与原装置比较,具有的优点是 .
(3)待燃烧完毕,试管冷却后,小丽将试管倒立于水中,取下橡皮塞,可观察到试管中的现象为 ;通过此实验可得出的一个结论是 .
查看习题详情和答案>>

(1)试管内可观察到的现象为
(2)改进后的装置与原装置比较,具有的优点是
(3)待燃烧完毕,试管冷却后,小丽将试管倒立于水中,取下橡皮塞,可观察到试管中的现象为
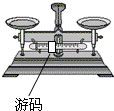 小明在某探究性实验中需要称取一未知质量、具有强烈腐蚀性、易潮解的氢氧化钠(NaOH)固体,以下是其实验操作步骤及相关记录:
小明在某探究性实验中需要称取一未知质量、具有强烈腐蚀性、易潮解的氢氧化钠(NaOH)固体,以下是其实验操作步骤及相关记录:①从仪器室领取如图仪器;
②调整仪器至平衡状态;
③在仪器的左右盘上各放一张同样大小的纸;
④将待称量的氢氧化钠固体放在仪器右盘的纸上;
⑤在左盘上依次加上5g、10g两个砝码,移动游码使仪器处于平衡状态,读取游码刻度值与两个砝码质量相加得到氢氧化钠固体为16.7888g;
回答以下问题:
(1)写出①中仪器名称
(2)氢氧化钠中氢元素的质量分数为
(3)写出步骤②的具体操作
(4)以上步骤中具有明显科学错误的是(填序号)
 小雅同学通过学习,对空气和氧气有了一定的了解:
小雅同学通过学习,对空气和氧气有了一定的了解:A.工业制氧气的原理是分离液态空气,其方法是首先将空气通过
加压降温
加压降温
处理后转化成液态空气,然后略微升温就可以使其中的氮气
氮气
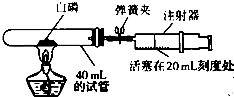
(填“氧气”或“氮气”)先逸出.(已知氧气的沸点是-183℃,氮气的沸点是-196℃)B.为验证空气中氧气的含量,小雅同学选用40mL的试管和量程足够大且润滑效果很好的注射器等作器材(如图).将足量的比红磷更易燃烧的白磷放入试管,用橡皮塞塞紧管口,夹紧弹簧夹.点燃酒精灯,使白磷在试管中燃烧(产物为五氧化二磷),燃烧结束待试管冷却后松开弹簧夹,观察现象.
(1)实验开始前,小雅打开弹簧夹,将注射器活塞从20mL刻度处推至15mL处,然后松开活塞,观察到
活塞退回20mL刻度
活塞退回20mL刻度
的现象,说明该装置气密性良好.(2)实验中,在松开弹簧夹前,试管中可以观察到白磷燃烧发出黄色火焰,放出大量热并产生
大量白烟
大量白烟
.(3)实验后,可以观察到注射器活塞会从原来的20mL刻度处慢慢向左移到约
③
③
处(橡皮管内空气忽略不计).①.4mL刻度 ②.8mL刻度 ③.12mL刻度 ④.16mL刻度
(4)如果装置中没有弹簧夹,重复该实验,则在整个实验中,注射器活塞
先向右后向左
先向右后向左
移动,最后停留在约8
8
mL处(橡皮管内空气忽略不计).C.实验室中检验氧气时小雅发现:收集的氧气占集气瓶容积的70%(空气占30%)时,能使带火星的木条复燃.那么,使带火星的木条复燃的氧气浓度的最低值是多少呢?
小雅对此展开探究:
第一组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积10%、20%、30%、40%、50%的水.用排水法收集氧气,恰好把5只集气瓶中的水排去.将带火星的木条依次插入①~⑤号瓶中,记录实验现象.
小雅在第一组实验的基础上又做了第二组和第三组实验,数据和现象见下表.
| 第一组 | 第二组 | 第三组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| 收集的O2占容积的体积分数(%) | 10 | 20 | 30 | 40 | 50 | 3l | 33 | 35 | 37 | 39 | 34 |
| 带火星木条的 状况 | 微亮 | 亮 | 很亮 | 复燃 | 复燃 | 很亮 | 很亮 | 复燃 | 复燃 | 复燃 | 很亮 |
收集的氧气占容积的体积分数最低为
35
35
%时,可使带火星的木条复燃,这时集气瓶中氧气体积分数是49或48
49或48
%(计算结果保留整数).