网址:http://m.1010jiajiao.com/timu3_id_1232375[举报]
| |||||||||||||||||||||||||||||||
本题对应于“物质结构与性质”选修模块的内容。
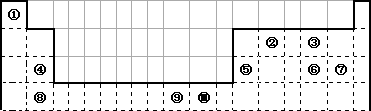
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
| Z |
|
|
|
| |||||||||||||
|
|
| M | L | Q | R |
|
| ||||||||||
| D | A |
|
| T | X | Y |
| ||||||||||
| E |
|
|
|
|
|
|
|
| J |
|
|
|
|
|
|
|
|
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LX2分子的电子式是_________,MY3分子是_________(填“极性分子”或“非极性分子”)。
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
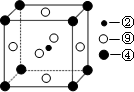
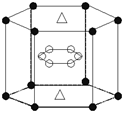
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最
高记录。右图中所示的是该化合物的晶体结构单元。图中上,下
底面中心“Δ”处的原子是_______(填元素符号)。
查看习题详情和答案>>
本题对应于“物质结构与性质”选修模块的内容。
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
|
Z |
|
|
|
|
|||||||||||||
|
|
|
M |
L |
Q |
R |
|
|
||||||||||
|
D |
A |
|
|
T |
X |
Y |
|
||||||||||
|
E |
|
|
|
|
|
|
|
|
J |
|
|
|
|
|
|
|
|
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LX2分子的电子式是_________,MY3分子是_________(填“极性分子”或“非极性分子”)。
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
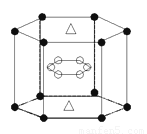
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最
高记录。右图中所示的是该化合物的晶体结构单元。图中上,下
底面中心“Δ”处的原子是_______(填元素符号)。
查看习题详情和答案>>
(12分)本题对应于“物质结构与性质”选修模块的内容。
下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。
| Z | |||||||||||||||||
| M | L | Q | R | ||||||||||||||
| D | A | T | X | Y | |||||||||||||
| E | J | ||||||||||||||||
(1)Y分别与D、E形成的化合物中熔点较高是_________(用具体物质的化学式表示)。
(2)LX2分子的电子式是_________,MY3分子是_________(填“极性分子”或“非极性分子”)。
 (3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
(3)由J、L、R三种元素形成的某种配位化合物,常温下该化合物具有挥发性,化学式为J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是__________________; J(LR)4固态时属于_________晶体(填晶体类型)
(4)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最
高记录。右图中所示的是该化合物的晶体结构单元。图中上,下
底面中心“Δ”处的原子是_______(填元素符号)。
查看习题详情和答案>>