摘要:⑥ 24.下图是实验室里用加热高锰酸钾的方法制取氧气的实验装置图. (1) ① ② ③ ④ ⑤ ⑥ ⑦ (2)用一团棉花放在靠近试管口的地方.目的 (3)将导管口伸入盛满水的标号为⑤的瓶里.开始收集氧气的适宜时刻是 (4)待瓶内的水排完.用玻璃片在水面下盖住瓶口.把集气瓶移出水面后放置在实验桌面上.放置的方法是 原因是 (5)停止加热时先把导气管移出水面.然后再熄灭酒精灯其原因是 25.如下图所示.这是用排水法收集到的无色气体.据此请你判断与这种气体相关的物理性质和化学性质.
网址:http://m.1010jiajiao.com/timu3_id_121288[举报]
空气质量日报的主要内容包括:首要污染物、空气污染指数和空气质量级别.
空气污染与空气质量级别的对应关系(表1)
| 空气污染指数 | O~50 | 5l~100 | 101~1 50 | 151~200 | 201~250 | 251~300 | >300 |
| 空气质量状况 | 优 | 良 | 轻度污染 I | 轻度污染 I | 中度污染 I | 中度污染 II | 重度 污染 |
| 空气质量 级别 | I | II | III | III | Ⅳ | Ⅳ | V |
| 城市 | 首要污染物 | 空气污染指数 | 空气质量级别 |
| 上海 | 可吸入颗粒物 | 111 | III轻度污染I |
| 天津 | 可吸入颗粒物 | 82 | |
| 昆明 | 二氧化硫 | 61 | II 良 |
| 海口 | 24 | I 优 |
(1)上述城市中易出现酸雨的城市是______,写出形成酸雨的气体与氢氧化钠溶液反应的化学方程式______.
(2)请依据表1和表2中的内容,确定当日天津的空气质量级别,并填在表2的空格里. 查看习题详情和答案>>
为了测定某种碳酸钠晶体(Na2CO3?xH2O)的x值,某学生将碳酸钠晶体放入坩埚中加热至不含结晶水,发生的反应为 Na2C03?xH2O Na2CO3+xH2O
Na2CO3+xH2O
实验测得的数据如下表:
| 坩埚的质量/g | 19.50 |
| 坩埚+碳酸钠晶体的质量/g | 24.14 |
| 坩埚+无水碳酸钠的质量/g | 21.62 |
(1)酸、碱、盐溶解性表是学习化学的重要工具.右表列出了“部分酸、碱、盐在20℃时的溶解性”.请按下列要求填写有关内容:
查溶解性:Cu(OH)2______.
写化学式:一种挥发性酸______.
判断:NaNO3与BaCl2溶液能否发生反应?______
(填“是”或“否”);理由是______;
写出铁或铝与表中的一种盐反应的化学方程式:______
(2)生产光滑纸张使用的“钡白”有一种制法,①用盐酸处理碳酸钡;②向所得溶液加入硫酸.写出“钡白”的主要成分的化学式:______;写出反应②的化学方程式:______
(3)①浓硫酸和稀硫酸,在实验室中敞口放置,它们的质量和放置天数的关系如右下图.
a、b曲线中表示浓硫酸的是(填字母序号)______;理由是______.
②下图是两种稀释浓硫酸的操作:
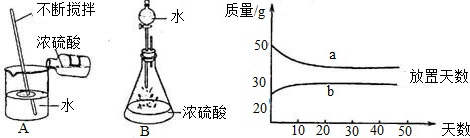
上面两图中,稀释浓硫酸操作正确的是(填序号)______,A图中玻璃棒的作用是______.B图中玻璃导管的作用是______.
(4)①某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸.若要清洗100kg的这种石油产品,理论上需要NaOH______kg.
②石化厂进行了技术改造,改用Ca(OH)2中和这些残余硫酸.每处理100kg这种产品,可以节约多少经费?
NaOH和Ca(OH)2的市场价格如下表:
| 名称 | NaOH | Ca(OH)2 |
| 价格(元/kg) | 24.00 | 6.00 |
实验室用98%的浓硫酸配制成稀硫酸,并与锌粒反应制取氢气.
(1)查阅资料.
20℃时不同质量分数硫酸的密度(g/mL)

分析以上数据,可以得出结论(写2条)
①________________;
②________________.
(2)计算.
配制200 g 24.5%的稀硫酸,需________g 98%浓硫酸和________g水.实际操作时,取98%浓硫酸________mL(精确到1 mL).
(3)配制稀硫酸溶液时,某同学用50 mL量筒量取所需浓硫酸的体积时,采取俯视量筒内液体刻度线的方法,则实际量取的浓硫酸的体积________(填“大于”、“等于”或“小于”)所需体积.