摘要: 已知硫酸的化学式为H2SO4.计算: (1)硫酸的相对分子质量是多少? (2)硫酸中硫元素与氧元素的质量比是多少? (3)硫酸中氢元素的质量分数是多少?
网址:http://m.1010jiajiao.com/timu3_id_118957[举报]
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)测定过程中发生反应的化学方程式为 ;
(2)从以上数据可知,最后剩余的0.6g固体的成分是 ;这六次实验中,第 次加入稀硫酸时样品中的镁已经完全反应;表格中,m= .
(3)计算合金样品中镁的质量分数.
(4)计算所用稀硫酸中H2SO4的质量分数. 查看习题详情和答案>>
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)从以上数据可知,最后剩余的0.6g固体的成分是
(3)计算合金样品中镁的质量分数.
(4)计算所用稀硫酸中H2SO4的质量分数. 查看习题详情和答案>>
某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
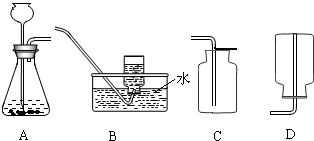
(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式 ; ;
上述可用于收集二氧化碳装置是 (用装置字母序号填空).
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三: (请补充完成假设三).
②实验探究:(填写表中空格)
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后, (填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m
g(选填>、<或=),则假设二成立;若m
g(选填>、<或=),则假设三成立.
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论. 查看习题详情和答案>>

(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳
的化学方程式
上述可用于收集二氧化碳装置是
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.氢气还原氧化铜除生成铜外还可能生成氧化亚铜(Cu2O);Ⅱ.Cu和Cu2O均为不溶于水的红色固体;Ⅲ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含Cu;假设二:红色固体只含Cu2O;
假设三:
②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 |
| b.取少量红色固体加入到足量硫酸溶液中 | 假设二和假设三均成立 |
| 64W |
| 144 |
| 64W |
| 144 |
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论. 查看习题详情和答案>>
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)测定过程中发生反应的化学方程式为:
(2)从以上数据可知,最后剩余的0.6g固体的成分是
(3)计算合金样品中镁的质量分数
查看习题详情和答案>>
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
Mg+H2SO4=MgSO4+H2↑
Mg+H2SO4=MgSO4+H2↑
.(2)从以上数据可知,最后剩余的0.6g固体的成分是
铜
铜
;这六次实验中,第5
5
次加入稀硫酸时样品中的镁已经完全反应;表格中,m=2.5g
2.5g
.(3)计算合金样品中镁的质量分数
80%
80%
(只写答案,不需要写计算过程).某化学课外兴趣小组探究氢气还原氧化铜的反应,有如下实验装置:
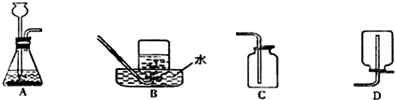
(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳的化学方程式
(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.Cu和Cu2O均为不溶于水的红色固体;Ⅱ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含有Cu;假设二:红色固体只含Cu2O;
假设三:
②实验探究:(填写表中空格)
③数据处理:甲同学称取Wg红色固体加入到足量硫酸溶液中使其充分反应后,
g(选填>、<或=),则假设二成立;若m
g(选填>、<或=),则假设三成立.
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.
查看习题详情和答案>>

(1)上述A装置可用于实验室制取氢气和二氧化碳,请分别写出实验室制取氢气和二氧化碳的化学方程式
Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
;CaCO3+2HCl=CaCl2+H2O+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
.(2)请你参与探究氢气还原氧化铜得到的红色固体的成分,完成下列各题:
已知信息:Ⅰ.Cu和Cu2O均为不溶于水的红色固体;Ⅱ.Cu2O+H2SO4=CuSO4+Cu+H2O
提出问题:红色固体含有什么物质?
①猜想假设:
假设一:红色固体只含有Cu;假设二:红色固体只含Cu2O;
假设三:
Cu和Cu2O的混合物
Cu和Cu2O的混合物
(请补充完成假设三).②实验探究:(填写表中空格)
| 实验操作 | 实验现象 | 实验结论 |
| a.取少量红色固体加入到足量硫酸溶液中 | 无明显现象 | 假设 1 1 成立 |
| b.取少量红色固体加入到足量硫酸溶液中 | 固体部分溶解,溶液由无色变为蓝色 固体部分溶解,溶液由无色变为蓝色 |
假设二和假设三均成立 |
过滤
过滤
(填操作名称)、洗涤、干燥,称量剩余红色固体质量为mg,通过计算,若m=
=
| 64w |
| 144 |
>
>
| 64w |
| 144 |
④交流与反思:只要假设合理,实验方法正确,根据实验现象和数据就能得出结论.