网址:http://m.1010jiajiao.com/timu3_id_103294[举报]
【查阅资料】
①2NaHCO3
| ||
| ||
②浓硫酸常用于吸收水蒸气和氨气.
③碱石灰是固体氢氧化钠和氧化钙的混合物,不与氨气反应.
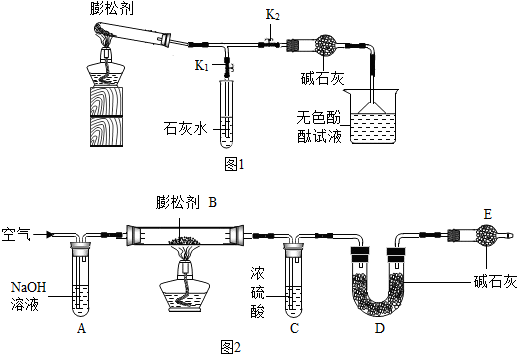
实验I:探究膨松剂的成分
按如图1所示连接好装置(夹持仪器略去,下同).
(1)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. 关闭K1,打开K2 |
装置的气密性良好. | |
| ② | 点燃酒精灯. 打开K1,关闭K2. |
试管中白色固体减少, 澄清的石灰水变浑浊 澄清的石灰水变浑浊 |
有二氧化碳生成,A中反应的化学方程式为 CO2+Ca(OH)2=CaCO3↓+H2O CO2+Ca(OH)2=CaCO3↓+H2O . |
| ③ | 打开K2,关闭K1. | 无色酚酞试液变红 | 有氨气生成. |
| ④ | 继续充分加热. | 试管中仍有固体 | |
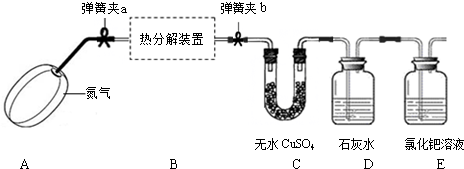
实验II:探究膨松剂受热产生气体的量
(1)测定二氧化碳的质量:如图2所示装置(气密性良好,各装置中的试剂为足量).
将8g膨松剂装入装置B中,通过测定实验前后装置
(2)测定氨气的质量:调整图2装置的连接顺序为
【解释与结论】同学们进一步对实验结果进行分析后,认为该膨松剂质量良好.
【反思与评价】实验II中,若没有装置E,造成测定结果可能会

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
【实验步骤】:
①连接好装置,
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置B的质量(/g) | 装置C的质量(/g) | |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g | ||
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(提示:相对分子质量分别为FeC2O4:144; H2O:18)
(5)实验过程中,鼓入氮气的目的是
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式
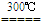 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O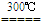 FeO+CO2↑+CO↑+2H2O
FeO+CO2↑+CO↑+2H2O【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁.你认为这种说法是否正确?请说出可能的理由
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么?
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式

5、铁的氧化物被CO还原所需的温度:

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):

【实验步骤】:
①连接好装置, ▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④ ▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| | 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g | ||
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了 ▲ ,FeC2O4·xH2O中x的值为 ▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了 ▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了 ▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18) ▲ ;
(5)实验过程中,鼓入氮气的目的是 ▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式 ▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由 ▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么? ▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式 ▲ .
(14分)草酸亚铁晶体(化学组成为FeC2O4·xH2O)是一种淡黄色晶体粉末,常用于照相显影剂及制药工业,是电池材料的制备原料.

5、铁的氧化物被CO还原所需的温度:
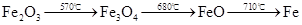
草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
【实验步骤】:
①连接好装置, ▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④ ▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
|
| 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了 ▲ ,FeC2O4·xH2O中x的值为 ▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了 ▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了 ▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18) ▲ ;
(5)实验过程中,鼓入氮气的目的是 ▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式 ▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由 ▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么? ▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式 ▲ .
查看习题详情和答案>>

5、铁的氧化物被CO还原所需的温度:

草酸亚铁晶体受热分解可以生成四种氧化物,为确定分解后的产物及x的值,某实验小组设计了如下实验装置并进行探究(酒精灯略去,不考虑装置中气体的质量,且无水CuSO4足量):
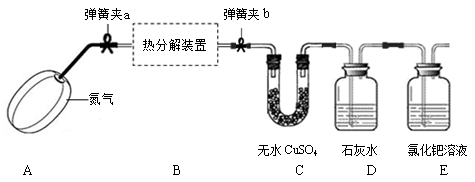
【实验步骤】:
①连接好装置, ▲ ;
②称量装置B(含两侧弹簧夹)、C的质量;
③在热分解装置中装入一定质量的草酸亚铁晶体,打开弹簧夹a、b,鼓入一段时间氮气;
④ ▲ ,用酒精灯加热热分解装置,直至晶体完全变成黑色,停止加热;
⑤打开弹簧夹a,继续通氮气至装置冷却,关闭弹簧夹a、b;
⑥再次称量装置B、C的质量.
【进行实验】:该小组同学按上述实验步骤进行实验,并记录了如下数据:
| | 装置B的质量(/g) | 装置C的质量(/g) |
| 实验前 | 145.8 | 168.2 |
| 实验后 | 140.4 | 170.0 |
| 热分解装置质量为136.8g |
【实验分析及数据处理】:
(1)实验过程中,装置C中固体颜色变为蓝色,说明草酸亚铁晶体分解生成了 ▲ ,FeC2O4·xH2O中x的值为 ▲ ;
(2)装置E出现黑色物质,说明草酸亚铁晶体分解生成了 ▲ ;
(3)装置C中澄清石灰水变浑浊,说明草酸亚铁晶体分解生成了 ▲ ;
(4)根据上表数据,计算反应后,热解装置中残留黑色物质的化学式;(3分)
(提示:相对分子质量分别为FeC2O4:144; H2O:18) ▲ ;
(5)实验过程中,鼓入氮气的目的是 ▲ ;
(6)实验后,热解装置中固体的颜色由淡黄色变成黑色,写出草酸亚铁晶体受热分解的化学方程式 ▲ ;
【反思应用】:
(7)有同学认为,实验中生成的CO和铁的氧化物会继续反应生成铁。你认为这种说法是否正确?请说出可能的理由 ▲ ;
(8)经过讨论,同学们一致认为上述实验装置有不足,你认为是什么? ▲ ;
(9)某些食品的包装袋中,常用氧化亚铁作为防伪试剂,一旦包装打开,立即变成红棕色,写出该反应的化学方程式 ▲ . 查看习题详情和答案>>