摘要:某学生设计还原CuO实验装置如图: (1)指出图中a.b.c.d仪器的名称 a b c d (2)写出A.B两处发生化学反应的字母表达式: A B (3)指出整个装置中的错误 ① ② ③ ④ ⑤ ⑥
网址:http://m.1010jiajiao.com/timu3_id_103130[举报]
某同学设计了一套用电解水产生的氢气还原氧化物,并收集氧气的装置(如图)
根据装置图回答:图中装置中的三处错误的是
查看习题详情和答案>>

根据装置图回答:图中装置中的三处错误的是
正负极颠倒
正负极颠倒
、试管口没有略向下
试管口没有略向下
、A导管没有伸到试管底部,氧化铜的上方
A导管没有伸到试管底部,氧化铜的上方
;电解水中正极与负极产生的气体的质量的比为8:1
8:1
;氢气还原氧化铜的化学方程式为H2+CuO
Cu+H2O
| ||
. |
H2+CuO
Cu+H2O
;实验现象为
| ||
. |
黑色的物质变成红色的物质,试管口有水珠生成
黑色的物质变成红色的物质,试管口有水珠生成
.(1)请根据装置如图1,回答有关问题:
实验室用B、C装置制取氧气的化学方程式为
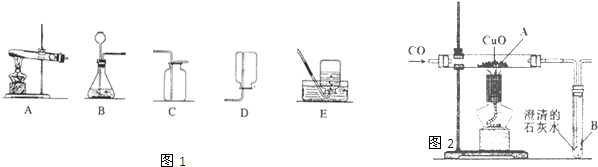
(2)某同学设计如图2所示的实验装置,进行一氧化碳还原氧化铜的实验.试回答:
①该装置存在的一个主要问题是
②实验开始时,是先给氧化铜加热,还是先通入一氧化碳?
③实验过程中,图中A处能观察到的实验现象是
④实验过程中,一氧化碳和氧化铜反应不仅能生成铜,还可能生成中间产物氧化亚铜(化学式为Cu2O).如果要对反应后A处残留固体的组成进行探究,试猜想残留固体的组成有哪几种可能?
查看习题详情和答案>>
实验室用B、C装置制取氧气的化学方程式为
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,若要用高锰酸钾制取氧气,应选用发生装置
| ||
A
A
(填字母),若要收集较纯净的氢气应选用装置E
E
(填字母),收集二氧化碳时,验满的方法是将燃着木条放在集气瓶口,若木条熄灭,则说明已收集满
将燃着木条放在集气瓶口,若木条熄灭,则说明已收集满
.(2)某同学设计如图2所示的实验装置,进行一氧化碳还原氧化铜的实验.试回答:
①该装置存在的一个主要问题是
未进行尾气处理
未进行尾气处理
,你的改进方法是在B装置后再加上一个燃着的酒精灯
在B装置后再加上一个燃着的酒精灯
.②实验开始时,是先给氧化铜加热,还是先通入一氧化碳?
先通入CO
先通入CO
.③实验过程中,图中A处能观察到的实验现象是
黑色粉末变成红色
黑色粉末变成红色
,发生反应的化学方程式为CO+CuO
Cu+CO2
| ||
CO+CuO
Cu+CO2
;B处观察到的实验现象是
| ||
澄清的石灰水变浑浊
澄清的石灰水变浑浊
.④实验过程中,一氧化碳和氧化铜反应不仅能生成铜,还可能生成中间产物氧化亚铜(化学式为Cu2O).如果要对反应后A处残留固体的组成进行探究,试猜想残留固体的组成有哪几种可能?
a.Cu b.Cu,CuO c.Cu,Cu2O,d.CuO,Cu2O e.Cu,Cu2O,CuO f.Cu2O
a.Cu b.Cu,CuO c.Cu,Cu2O,d.CuO,Cu2O e.Cu,Cu2O,CuO f.Cu2O
.
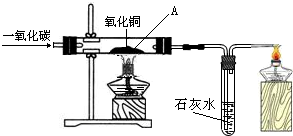 (2009?武威)如图所示,某同学用一氧化碳代替氢气还原氧化铜制取金属铜.请你参与他的探究过程,并回答下列问题.
(2009?武威)如图所示,某同学用一氧化碳代替氢气还原氧化铜制取金属铜.请你参与他的探究过程,并回答下列问题.(1)试写出一氧化碳与氧化铜反应生成金属铜和二氧化碳的化学方程式:
CO+CuO
Cu+CO2
| ||
CO+CuO
Cu+CO2
.
| ||
(2)该装置中,右边的酒精灯的作用是
将未参加反应的CO燃烧掉,防止污染空气
将未参加反应的CO燃烧掉,防止污染空气
.(3)实验结束后,该同学对A处残留固体的组成进行了探究.
查阅资料得知,由于给氧化铜加热温度不够或通入一氧化碳不足,反应不仅能生成铜,还可能生成中间产物氧化亚铜(化学式为Cu2O).氧化亚铜也是一种红色固体,难溶于水,可与稀硫酸发生如下反应:Cu2O+H2SO4═CuSO4+Cu+H2O
①残留固体的组成有哪几种可能?(用化学式表示)
a.Cu;b.Cu、CuO;c.Cu、Cu2O;d.CuO、Cu2O;e.Cu、Cu2O、CuO;f.Cu2O
a.Cu;b.Cu、CuO;c.Cu、Cu2O;d.CuO、Cu2O;e.Cu、Cu2O、CuO;f.Cu2O
.②请你设计实验,证明氧化铜是否全部转化为金属铜.
| 实验内容和步骤 | 观察到的实验现象和结论 |
化学是一门以实验为基础的科学.
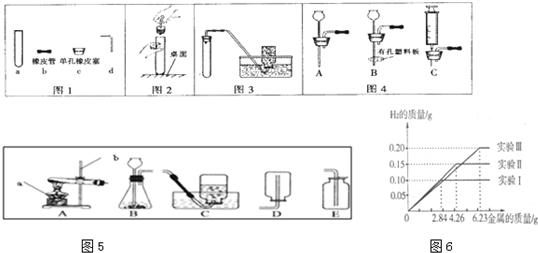
(1)根据图1回答:①写出a的名称
(2)采用图2所示操作可能造成的后果之一是
(3)利用图3装置(夹持装置未画出)能进行的实验是
(4)图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率.请从图4中选取
(5)实验室用图5中A装置制氧气的化学方程式是
(6)机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:①NO常温下是一种无色、难溶于水的气体,它的密度比空气略大;②NO常温下能与氧气迅速反应,生成红棕色的NO2气体:2NO2+O2═2NO2;③实验室常用铜与稀硝酸反应制取NO:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4X. 根据以上信息完成下列问题:
①物质X的化学式为
②若选择合适的装置来制取并收集NO气体,你选择图5中的发生装置是
③该小组的同学通过查阅资料还得知:a.NO容易和血红蛋白结合而使人中毒;b.NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是
④某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案二:2Cu+O2
2CuO,CuO+2HNO3═Cu(NO3)2+H2O.从环境保护的角度考虑,你认为较合理的方案是
(7)某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图象图6:试回答(计算结果精确到0.1%):
①写出实验中有关的化学方程式:
②实验I中铁参加反应的质量为
③稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少.
查看习题详情和答案>>

(1)根据图1回答:①写出a的名称
试管
试管
;②在连接c和d时,使d较易插入c中的措施是用水湿润
用水湿润
;(2)采用图2所示操作可能造成的后果之一是
试管破裂
试管破裂
;(3)利用图3装置(夹持装置未画出)能进行的实验是
CD
CD
(选填序号);A.用高锰酸钾制氧气; B.用石灰石与稀盐酸制二氧化碳;C.用锌与稀硫酸制氢气; D.用双氧水与二氧化锰制氧气.(4)图3中的气体发生装置虽然简单,操作方便,但无法控制反应速率.请从图4中选取
B或C
B或C
(选填序号)与图1中a组装成新的气体发生装置,以达到控制反应速率的目的.(5)实验室用图5中A装置制氧气的化学方程式是
2KClO3
2KCl+3O2↑
| ||
| △ |
2KClO3
2KCl+3O2↑
,反应结束后冷却,往试管中加入足量的水,搅拌、过滤,得到黑色粉末.该黑色粉末与过氧化氢接触有大量气泡产生,反应的化学方程式是
| ||
| △ |
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
,黑色粉末在反应中的作用是
| ||
催化
催化
.用E装置收集氧气的依据是氧气的密度大于空气的密度
氧气的密度大于空气的密度
,检验氧气是否集满的方法是将带火星的木条放在集气瓶口,木条复燃说明已满
将带火星的木条放在集气瓶口,木条复燃说明已满
.(6)机动车排放的尾气是空气的重要污染源,其成分之一是NO.某化学兴趣小组的同学在查阅资料后得知:①NO常温下是一种无色、难溶于水的气体,它的密度比空气略大;②NO常温下能与氧气迅速反应,生成红棕色的NO2气体:2NO2+O2═2NO2;③实验室常用铜与稀硝酸反应制取NO:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4X. 根据以上信息完成下列问题:
①物质X的化学式为
H2O
H2O
. ②若选择合适的装置来制取并收集NO气体,你选择图5中的发生装置是
B
B
,收集装置是C
C
.③该小组的同学通过查阅资料还得知:a.NO容易和血红蛋白结合而使人中毒;b.NO能抗击侵入人体的微生物,并能阻止癌细胞的繁殖和肿瘤细胞的扩散.综合分析①和②的信息,你得到的启示是
任何物质都具有两面性
任何物质都具有两面性
④某化工厂准备生产Cu(NO3)2,以铜和稀硝酸为主要原料设计了两种方案:
方案一:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑十4X;
方案二:2Cu+O2
| ||
方案二
方案二
.从经济角度考虑选择此方案的理由是产生相同质量的硝酸铜所消耗的稀硝酸少
产生相同质量的硝酸铜所消耗的稀硝酸少
.(7)某化学调查小组的同学到钢铁厂做社会调查.他们抽取组成完全相同的质量为2.84g、4.26g、6.23g的三份钢样(假设钢样中只含铁和碳),分别加入100g稀硫酸中进行实验(实验I、Ⅱ、Ⅲ),充分反应后,将得到的实验数据绘制出如图象图6:试回答(计算结果精确到0.1%):
①写出实验中有关的化学方程式:
Fe+H2SO4═FeSO4+H2↑
Fe+H2SO4═FeSO4+H2↑
.②实验I中铁参加反应的质量为
2.8g
2.8g
.③稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少.
 某同学设计如图所示的实验装置,进行一氧化碳还原氧化铜的实验.试回答:
某同学设计如图所示的实验装置,进行一氧化碳还原氧化铜的实验.试回答: