摘要:为了探究“H2O2生成O2的快慢与什么因素有关 .某研究性学习小组做了以下实验:常温下.在两瓶同质量的H2O2溶液中分别加入同质量的MnO2和红砖粉.测量各生成一瓶同体积O2所需的时间.记录如下: 实验编号 1 2 反应物 6% H2O2 6% H2O2 催化剂 1g MnO2 1g 红砖粉 时 间 35s 152s 分析以上数据.你得出的结论是 .你认为“H2O2生成O2的反应速率还与哪些因素有关 ?例如: .
网址:http://m.1010jiajiao.com/timu3_id_10108[举报]
为了探究“H2O2生成O2的快慢与什么因素有关”,某研究性学习小组做了以下实验:常温下,在两瓶同质量的H2O2溶液中分别加入同质量的MnO2和红砖粉,测量各生成一瓶同体积O2所需的时间.记录如下:
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g MnO2 | 1g红砖粉 |
| 时间 | 35s | 152s |
为了探究“H2O2生成O2的快慢与什么因素有关”,某研究性学习小组做了以下实验:常温下,在两瓶同质量的H2O2溶液中分别加入同质量的MnO2和红砖粉,测量各生成一瓶同体积O2所需的时间.记录如下:
分析以上数据,你得出的结论是______,你认为“H2O2生成O2的反应速率还与哪些因素有关”?(举一例)例如:______.
查看习题详情和答案>>
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g MnO2 | 1g红砖粉 |
| 时间 | 35s | 152s |
为了探究“H2O2生成O2的快慢与什么因素有关”,某研究性学习小组做了以下实验:常温下,在两瓶同质量的H2O2溶液中分别加入同质量的MnO2和红砖粉,测量各生成一瓶同体积O2所需的时间.记录如下:
分析以上数据,你得出的结论是,你认为“H2O2生成O2的反应速率还与哪些因素有关”?(举一例)例如:.
查看习题详情和答案>>
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g MnO2 | 1g红砖粉 |
| 时间 | 35s | 152s |
18、为了探究“H2O2生成O2的快慢与什么因素有关”,某研究性学习小组做了以下实验:常温下,在两瓶同质量的H2O2溶液中分别加入同质量的MnO2和红砖粉,测量各生成一瓶同体积O2所需的时间.记录如下:
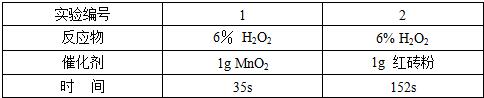
分析以上数据,你得出的结论是
查看习题详情和答案>>
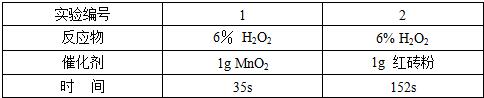
分析以上数据,你得出的结论是
H2O2生成O2的快慢与催化剂的种类有关
,你认为“H2O2生成O2的反应速率还与哪些因素有关”?(举一例)例如:可能与反应物的浓度有关.(其他答案合理亦可)
.研究性学习小组选择“H2O2溶液反应生成氧气的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程: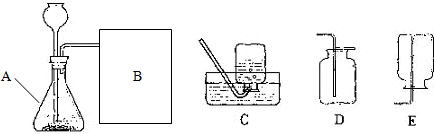
[假设]H2O2溶液生成氧气的快慢与催化剂的种类有关.
[实验方案]常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和碎瓷片,测量各生成一瓶(相同体积)O2所需要的时间.
[进行实验]下图是他们进行实验的装置图,发生装置中A仪器的名称是:
[实验记录]
(1)H2O2中氧元素的化合价为
(2)表中实验1中反应物H2O2溶液中溶质的质量分数(w%)应 为
(3)写出实验2中反应的文字表达式:
[结论]该探究过程得出的结论是:H2O2溶液生成氧气的快慢与催化剂的种类有关.
[反思](1)H2O2溶液在常温下分解缓慢,加入MnO2或碎瓷片后反应明显加快.若要证明MnO2是该反应的催化剂,补充设计了两方面的探究实验:第一方面的实验操作中包含了两次称量,其目的是
查看习题详情和答案>>

[假设]H2O2溶液生成氧气的快慢与催化剂的种类有关.
[实验方案]常温下,在两瓶相同体积的H2O2溶液中分别加入相同质量的MnO2和碎瓷片,测量各生成一瓶(相同体积)O2所需要的时间.
[进行实验]下图是他们进行实验的装置图,发生装置中A仪器的名称是:
锥形瓶
锥形瓶
,此实验中B处适宜采用的气体收集方法是(填序号):C
C
.[实验记录]
| 实验编号 | 1 | 2 |
| 反应物 | w%H2O2溶液 | 6%H2O2溶液 |
| 催化剂 | 1g碎瓷片 | 1gMnO2 |
| 时间 | 152s | 45s |
-1
-1
.(2)表中实验1中反应物H2O2溶液中溶质的质量分数(w%)应 为
6%
6%
.(3)写出实验2中反应的文字表达式:
过氧化氢
水+氧气
| 二氧化锰 |
过氧化氢
水+氧气
.| 二氧化锰 |
[结论]该探究过程得出的结论是:H2O2溶液生成氧气的快慢与催化剂的种类有关.
[反思](1)H2O2溶液在常温下分解缓慢,加入MnO2或碎瓷片后反应明显加快.若要证明MnO2是该反应的催化剂,补充设计了两方面的探究实验:第一方面的实验操作中包含了两次称量,其目的是
探究二氧化锰在反应前后质量不变
探究二氧化锰在反应前后质量不变
;第二方面的探究实验是利用“实验2”反应后试管内的剩余物继续实验.接下来的实验操作是过滤、洗涤、干燥后,将得到的固体加入盛有6%H2O2溶液的试管中,其目的是探究二氧化锰在反应前后化学性质不变
探究二氧化锰在反应前后化学性质不变
.